Questões de Concurso
Foram encontradas 49.808 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
1) Um circuito com resistores, capacitores e indutores em série deve ter suas impedâncias somadas.
2) O relé é um dispositivo de proteção que se rompe quando uma corrente excessiva passa por ele.
3) Um circuito com fator de potência atrasado é um circuito predominantemente indutivo.
4) Dependendo da frequência aplicada, o mesmo circuito pode se comportar de forma predominantemente indutiva ou predominantemente capacitiva.
Estão corretas, apenas
1) Potência reativa
2) Admitância
3) Resistividade
4) Relutância magnética
5) Fluxo magnético
( ) Weber
( ) Ampére espira por weber
( ) Volt-ampère reativo
( ) Siemens
( ) Ohm por metro
A sequência correta, de cima para baixo, é
A figura abaixo mostra uma representação simplificada do ciclo biogeoquímico do nitrogênio:
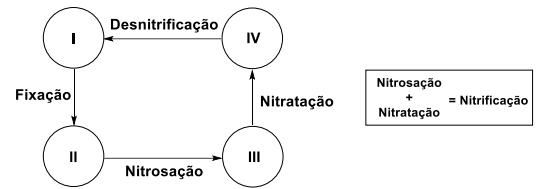
As espécies I, II, III e IV são, respectivamente:
Observe as estruturas dos ácidos abaixo:
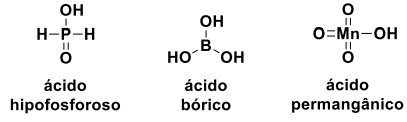
Sobre esses ácidos, analise as seguintes afirmações:
1. O ácido hipofosforoso possui três hidrogênios ionizáveis.
2. No ácido permangânico, o número de oxidação do Mn é +7.
3. O ácido bórico possui hibridação sp2 e geometria trigonal plana.
4. Devido à presença do metal, o ácido permangânico é o mais fraco.
Estão corretas, apenas:
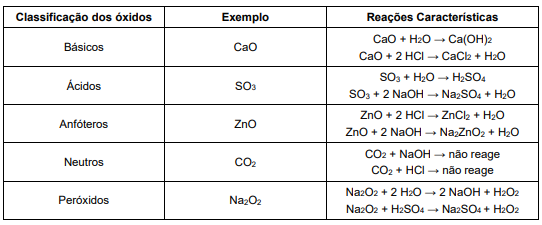
Ao observar a tabela, o professor precisou explicar ao estudante que um exemplo estava errado e não correspondia à classificação sugerida. A categoria cujo exemplo está incorreto é a dos óxidos:
Usado para a limpeza de peças e ferramentas, o ácido muriático é uma solução impura de ácido clorídrico e pode ser encontrado em lojas de materiais de construção. Com o objetivo de determinar a concentração de um lote desse produto em termos de porcentagem de HCl (m/V), um químico reagiu uma alíquota de 50mL do ácido muriático comercial com carbonato de cálcio em excesso, conforme a reação:
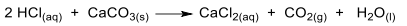
Nesse experimento, o volume coletado de CO2 foi 6,15L a 27oC e 1 atm. Qual é a porcentagem de HCl (m/V) na amostra de ácido muriático?
Massas molares (g/mol): H = 1; C = 12; O = 16; Cl = 35,5; Ca = 40
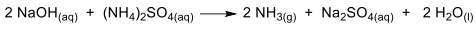
Considere que, em uma indústria química, são colocados em um reator 60kg de NaOH, 66kg de (NH4)2SO4 e água suficiente para solubilizar os reagentes. A reação ocorre até que um dos reagentes seja completamente consumido. Considerando as CNTP, o volume obtido de NH3(g) é:
Massas molares (g/mol): H = 1; O = 16; N = 14; Na = 23; S = 32

Considerando que essa reação tem um rendimento de 90%, calcule a massa de alumínio necessária para a produção de 11,2 kg de ferro para solda.
Massas molares (g/mol): O = 16; Al = 27; Fe = 56.

A reação não está balanceada. Faça o balanceamento, considerando os menores inteiros como coeficientes reacionais. A soma desses coeficientes é igual a:
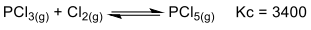
Considere que a reação acima está em equilíbrio e que as concentrações de PCl3 e Cl2 são 1,0 x 10-3 molL-1 e 1,0 x 10-2 molL-1 , respectivamente. Nessas condições, a pressão de PCl5 no equilíbrio será:
Considere os dados da tabela abaixo:

De acordo com os dados acima, o ânion que atua como base mais forte é:
Dados: log 2 = 0,3 e log 3 = 0,48
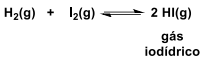
Considere um reator de 10L em que inicialmente são colocados 0,9 mol de H2(g) e 0,9 mol de I2(g) na temperatura T. Quando o equilíbrio for atingido, a concentração molar de HI(g) no equilíbrio será de:
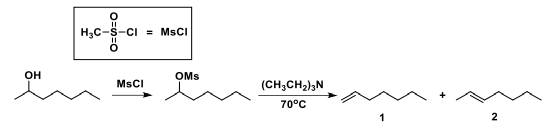
Sobre a etapa de eliminação, é correto afirmar que: