Questões de Concurso
Sobre química
Foram encontradas 13.691 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Qual substância pode ser preparada pela reação entre benzeno e clorofórmio na presença de AlCl3?
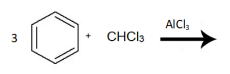
( ) É uma molécula planar com a forma de um hexágono regular.
( ) No benzeno, todos os átomos de carbono são hibridizados sp2 e cada átomo de carbono tem um orbital p perpendicular ao plano do anel.
( ) Na molécula de benzeno, todos os ângulos de ligação C – C – C são de 109°.
( ) Quando se aquece o benzeno com uma mistura de ácido nítrico e ácido sulfúrico concentrados, um grupo nitro substitui um dos átomos de hidrogênio ligados ao anel.
( ) O tratamento de benzeno com bromo na presença de FeCl3 resulta na formação de bromobenzeno e HBr.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
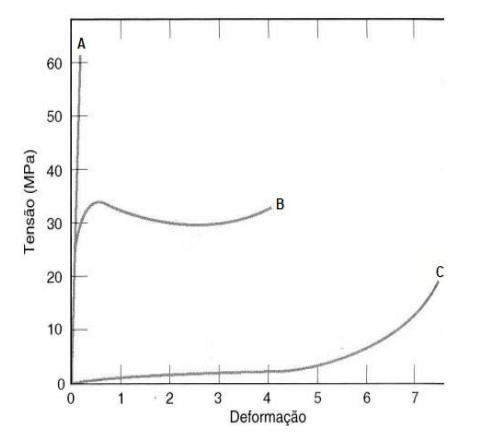
Figura 1
No que se refere ao cenário atual do Brasil e do mundo, julgue o item.
O chamado efeito estufa é ampliado pela emissão de
gases poluentes na atmosfera, fator este que é
resultante do modelo de industrialização adotado
mundialmente.
Um dos radionuclídeos do Radônio é 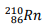 que decai emitindo
partículas alfa (α) para um dos isótopos do Polônio.
que decai emitindo
partículas alfa (α) para um dos isótopos do Polônio.
Uma reação que representa esse processo de desintegração nuclear é dada por:
Após a leitura, assinale a opção que mostra O SOMATÓRIO DOS COEFICIENTES ESTEQUIOMÉTRICOS, expressos com os menores inteiros, da reação citada na etapa 1 acima, A GEOMETRIA MOLECULAR da arsina e o ESTADO DE OXIDAÇÃO (Nox) do arsênio no ácido arsênico, respectivamente:
Um frasco contém uma mistura em equilíbrio de X2(g) e X atômico, segundo a reação:
X2(g) ⇌ 2 X(g)
A pressão de equilíbrio encontrada foi de 2,4 atm em certa condição de temperatura e volume. Se X2 gasoso a
uma pressão parcial de 3 atm for adicionado à mistura em equilíbrio acima, a volume e temperatura constantes,
a nova pressão de equilíbrio será de 5,66 atm, sendo que, no processo, a pressão do X (g) atômico aumenta
65% em relação ao valor da condição inicial. Nestas condições, assinale a opção que mostra O VALOR MAIS
PRÓXIMO DE Kp para a decomposição de X2(g), na mesma temperatura:
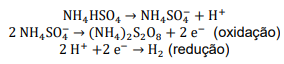
A hidrólise do persulfato de amônio forma H2O2:
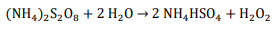
Se a eficiência do processo eletrolítico é de 60% assinale a opção que mostra a INTENSIDADE DE CORRENTE necessária para produzir 97 g de H2O2 por hora: Dados eventualmente necessários: constante de Faraday = 96500 C/mol; massas molares (g/mol): N = 14; O = 16; H = 1; S = 32.
I. Suporta elevadas temperaturas, tem formato arredondado e permite aquecimento uniforme. Essa vidraria é utilizada em processos de destilação, sistemas de evaporação a vácuo e refluxo;
II. É utilizada para medição de volumes, em que não é requerida precisão, e a presença de um bico facilita a transferência de líquidos. Essa vidraria é de uso geral e é útil para realizar misturas e dissolver substâncias em experimentos;
III. É utilizada para medir e transferir líquidos, podendo ser possível controlar o escoamento do material, rápido ou por gotejamento, pois a torneira na extremidade da vidraria permite fazer esse controle. Essa vidraria é amplamente utilizada em titulações, para comportar a substância titulante;
IV. É utilizada para preparar soluções, armazená-las e realizar experimentos que necessitem de aquecimento. Em processos de titulação, essa vidraria geralmente é utilizada para comportar a substância que vai ser titulada.
Com base na análise dos itens I a IV, assinale a opção CORRETA:
I. Os efluentes não poderão conferir ao corpo receptor características de qualidade em desacordo com as metas obrigatórias progressivas, intermediárias e final do seu enquadramento;
II. O estudo de capacidade de suporte deve considerar, no mínimo, a diferença entre os padrões estabelecidos pela classe e as concentrações existentes no trecho desde a montante, estimando a concentração após a zona de mistura;
III. É vedado, nos efluentes, o lançamento dos Poluentes Orgânicos Persistentes - POPs, observada a legislação em vigor;
IV. O lançamento de efluentes em corpos de água, com exceção daqueles enquadrados na classe especial, não poderá exceder as condições e padrões de qualidade de água estabelecidos para as respectivas classes.
Assinale a opção CORRETA: