Questões de Concurso Sobre grandezas: massa, volume, mol, massa molar, constante de avogadro e estequiometria. em química
Foram encontradas 961 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
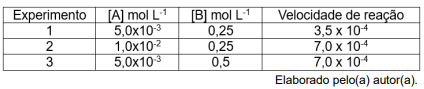
De acordo com os dados apresentados, a lei de velocidade para a reação estudada é:
Use: R = 0,082 atm . L . mol-1 K-1
Use: Massas Molares: O = 16,0 g mol-1; C = 12 g mol-1; H = 1 g mol-1; N = 14 g mol-1; Cl = 35,5 g mol-1
Massas Molares: O = 16,0 g mol-1; C = 12 g mol-1; H = 1 g mol-