Questões de Concurso
Sobre química
Foram encontradas 13.691 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
I. Alumínio-trimetil, sódio e potássio. II. Lítio, bromo e alumínio. III. Dietil-zinco, butil-lítio e alumínio-dietil cloreto. IV. Alumínio-etil sesquicloreto, cromo e alumínio-etil dicloreto.
Ca5(PO4)3 F + H3PO4 + H2O HF + Ca(H2PO4)2 . H2O (I)
Em um processo industrial, partiu-se de 1 tonelada de fluorapatita fazendo-a reagir com uma quantidade suficiente de ácido fosfórico obtendo-se, ao final, 2 toneladas do produto di-hidrogenofosfato de cálcio monohidratado. Pode-se, por esses dados, prever que a pureza do mineral utilizado, em percentual, era aproximadamente igual a:
(Dados, em g/mol: Ca= 40, P=31, O=16, H=1, F=19)
(Dados, em g/mol; H=1, S=32 e O=16; log 2=0,3)
(Dados em g/mol: Na= 23, O = 16, H = 1)
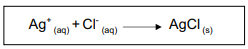
A porcentagem (%) de íons Cl- presente na amostra é: Dados: MMCl = 35,5 g mol -1
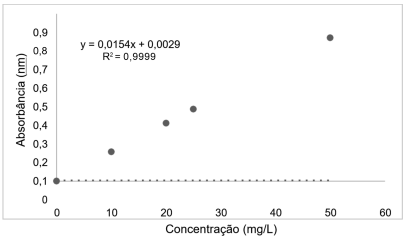
Após esse procedimento, o técnico fez a leitura de duas amostras A e B, com absorbâncias de 0,305 e 0,525 nm. Serão as concentrações das amostras, em mg/L, respectivamente: