Questões de Concurso
Sobre química
Foram encontradas 13.691 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Pesos moleculares: I=127 g/mol; K= 39 g/mol; O= 16 g/mol; C=12 g/mol.
Reações de neutralização são reações entre um ácido e uma
base que produzem sal e água, de acordo com os conceitos de
Arrhenius. O sal inorgânico formado é então um produto iônico
dessa reação que ao ter contato com a água é dissolvido liberando
no mínimo um cátion diferente de H+ e no mínimo um ânion
diferente de OH-. Considerando a dissolução de um sal em uma
solução aquosa neutra, assinale a alternativa correta.
As figuras a seguir ilustram quatro curvas de titulação volumétrica de neutralização (A, B, C e D), envolvendo ácidos e bases de concentrações iguais.
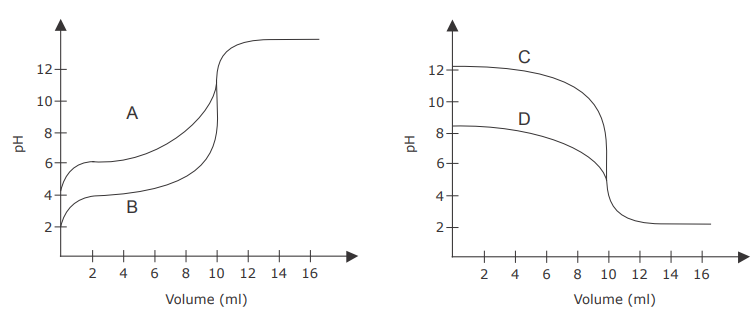
Em relação às curvas de titulação da figura, assinale V (verdadeiro) ou F (falso) em cada afirmativa a seguir.
( ) A curva "A" representa a titulação de um ácido fraco com uma base forte.
( ) A curva "B" representa a titulação de um ácido muito fraco com uma base forte.
( ) A curva "C" representa a titulação de uma base fraca com um ácido forte.
( ) A curva "D" representa a titulação de um ácido fraco com uma base forte.
A sequência correta é
Para a determinação colorimétrica de um composto "X" na faixa de concentração de 1 a 8 mg/L, um analista realizou a medida de absorvância para 4 padrões em um colorímetro de bancada. A curva de calibração preparada pelo analista pode ser visualizada na figura.
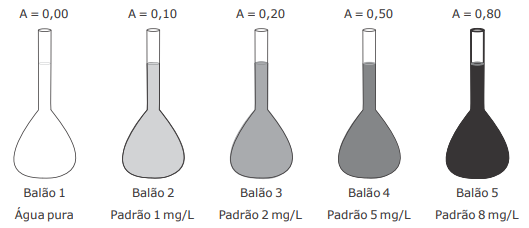
Sabendo que a análise do composto "X" deve apresentar absorvância no intervalo entre 0,10 e 0,80 e que o
rótulo da amostra contendo o composto "X" indica uma concentração de 2000 mg/L, considere as afirmativas
a seguir.
I - A amostra precisa ser diluída 100 vezes para que possa ser medida pelo método colorimétrico proposto no intervalo de concentração e absorvâncias mostrado na figura.
II - 1 mL da amostra deve ser pipetado em um balão volumétrico de 500 mL e o volume aferido com água desionizada, para que essa amostra possa ser medida pelo método colorimétrico proposto no intervalo de concentração e absorvâncias mostrado na figura.
III - 5 mL da amostra devem ser pipetados em um balão volumétrico de 500 mL e o volume aferido com água desionizada, para que essa amostra possa ser medida pelo método colorimétrico proposto no intervalo de concentração e absorvâncias mostrado na figura.
IV - 1 mL da amostra deve ser pipetado em um balão volumétrico de 250 mL e o volume aferido com água desionizada, para que essa amostra possa ser medida pelo método colorimétrico proposto no intervalo de concentração e absorvâncias mostrado na figura.
Está(ão) correta(s)
I - A absortividade molar de um composto aumenta com a sua concentração.
II - A absorvância e a absortividade molar do composto são inversamente proporcionais.
III - As dimensões do percurso ótico utilizado no colorímetro influenciam diretamente na quantidade de luz absorvida pelo composto.
IV - A absorvância medida para o composto de concentração "X" duplica, se a sua concentração passar para "4X" na medida colorimétrica com um percurso ótico de igual dimensão.
Está(ão) correta(s)
SOLUÇÃO 1 - 10 mL da solução estoque (2,010 mol/L) foi pipetado e transferido para um balão volumétrico de 100 mL, onde o volume foi completado com água desionizada.
SOLUÇÃO 2 - 5 mL da SOLUÇÃO 1 foi pipetado e transferido para um balão volumétrico de 50 mL, onde o volume foi completado com água desionizada.
As concentrações finais da SOLUÇÃO 1 e SOLUÇÃO 2 são, respectivamente,
O cloreto de prata (AgCl) é um sal pouco solúvel em água pura, com um produto de solubilidade (Kps) igual a 1,8x10-10. Quando em contato com a água, apresenta uma baixa concentração de íons Ag+(1,34x10-5 mol/L) e íons Cl- (1,34x10-5 mol/L) no equilíbrio químico em solução devido à reação
AgCl(s) ⇄ Ag+ (aq) + Cl- (aq)
Em qual das soluções a seguir o sal AgCl será mais
insolúvel, quando comparado com a água pura?
O quadro abaixo apresenta potenciais-padrão (E0) para semirreações de redução de cinco elementos.
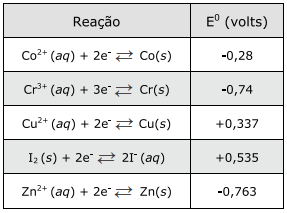
A ordem crescente de poder redutor conforme as
reações de redução acima é
Resíduos de metais pesados gerados em laboratório químico podem ser tratados por reação de precipitação com carbonato, geralmente na forma de calcário. O sólido obtido é filtrado em papel e armazenado, sendo que o líquido filtrado é neutralizado antes do descarte. Para a separação de resíduos dos íons metálicos Pb2+ , Cd2+ e Cu2+, a precipitação ocorre de acordo com as seguintes reações:

Em relação às reações de precipitação e seus produtos de solubilidade (Kps), considere as afirmativas a seguir.
I - Cu2+ é o íon mais insolúvel da mistura na precipitação com íon 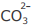
II - Pb2+ é o íon mais solúvel da mistura na precipitação com íon 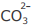
III - Cd2+ é mais insolúvel do que Cu2+ e Pb2+ na
precipitação com íon 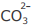
Está(ão) correta(s)
O ácido fosfórico é um reagente amplamente utilizado nas indústrias alimentícias, têxtil e metalúrgica. Na fabricação de fertilizantes, o H3PO4 também é frequentemente empregado na produção de superfosfatos. Em laboratórios de análises químicas, o H3PO4 é frequentemente utilizado para o preparo de soluções aquosas destinadas à realização de um grande número de procedimentos. Esse ácido se dissocia em água de acordo com as seguintes reações de hidrólise:
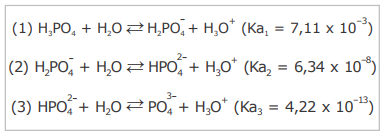
A partir das reações demonstradas acima, considere as seguintes afirmativas.
I - A partir da dissociação do H3PO4, três bases conjugadas são formadas na solução em equilíbrio químico.
II - A etapa (3) de dissociação libera a maior concentração de íons hidrônio (H3O+) na solução em equilíbrio químico.
III - A concentração do ânion 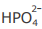 é maior que a concentração do ânion
é maior que a concentração do ânion 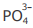 na solução em equilíbrio 4
químico.
na solução em equilíbrio 4
químico.
IV - A concentração do ânion 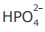 é maior que a concentração do ânion
é maior que a concentração do ânion 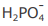 na solução em equilíbrio químico.
na solução em equilíbrio químico.
Estão corretas
( ) O eletrodo combinado possui dois eletrodos de referência (Ag/AgCl) que medem a diferença de potencial elétrico por meio da membrana de vidro.
( ) O eletrodo combinado possui um bulbo de vidro com um anel externo de prata metálica (Ag) sensível a íons H+.
( ) O termo eletrodo de vidro combinado é sinônimo de eletrodo de vidro, tendo a mesma estrutura e funcionamento.
( ) As principais interferências para esse tipo de eletrodo são os íons metálicos alcalinos, como o Na+, Li+ e K+.
A sequência correta é
A dureza da água é definida pela quantidade de alguns íons dissolvidos, como carbonatos, sulfatos, cálcio e magnésio. Para a determinação da dureza total, faz-se necessária a determinação destes íons de maneira seletiva. Como exemplo, a determinação de íons Ca2+ em águas envolve com frequência a titulação complexométrica com o reagente etilenodiaminotetra-acetato dissódico (Na2 EDTA).
Com esse propósito, um químico preparou uma solução do sal Na2EDTA di-hidratado (peso molecular = 372,0 g) pela dissolução de 0,140 g em 250 mL de água desionizada.
Com relação a essa solução preparada, qual sua concentração molar (mol/L)?
I - A concentração molar da solução de íon Fe2+ é 0,0005 mol/L.
II - A concentração molar da solução de FeSO4.7H2O é 0,005 mol/L.
III - A concentração percentual (massa/volume) da solução de íon Fe2+ é 13,9%.
IV - A concentração percentual (massa/volume) da solução de FeSO4.7H2O é 0,139%.
Está(ão) correta(s)
Para trabalhar em laboratórios químicos, devem ser levadas em conta muitas precauções e cuidados.
Assinale V (verdadeiro) ou F (falso) em cada afirmativa a seguir.
( ) A proteção para olhos é obrigatória em qualquer experimento.
( ) Em dias de muito calor, pode-se trabalhar de bermuda ou saia, desde que o avental seja bem comprido.
( ) Para introdução de tubos de vidro em rolhas perfuradas, é aconselhado lubrificar primeiramente o vidro e fazer uso de um pano ou luvas para segurá-los.
( ) Experiências que envolvam materiais muito tóxicos devem ser conduzidas em capelas de exaustão.
A sequência correta é
Em locais onde neva, é costume colocar sal (NaCl) sobre ruas e calçadas, pois facilita a fusão do gelo. Em um experimento de laboratório, os estudantes de uma classe de Química tentaram simular o que se observa, mas, nesse caso, comparando dois recipientes, um contendo gelo e sal, e outro, gelo e açúcar.
Analise as afirmativas a seguir em relação ao experimento dos estudantes.
I - Ambos os compostos usados dissolveram-se facilmente na água.
II - O sal foi mais eficiente no processo de fusão do gelo, pois um mol de NaCl tem o dobro de solutos do que um mol de açúcar.
III - O ponto de congelamento da água aumentou pelas interações entre ela e os solutos, em relação à água pura.
Está(ão) correta(s)