Questões de Concurso
Sobre química
Foram encontradas 13.691 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Dado: massa molar da glicose anidra = 180g/mol
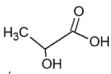
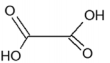
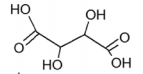
Ácido lático Ácido oxálico Ácido tartárico pKa = 3,85 pKa1= 1,25 ; pKa2 = 4,29 pKa1=3,04; pKa2=4,37
Em relação a esses ácidos, é CORRETO afirmar que
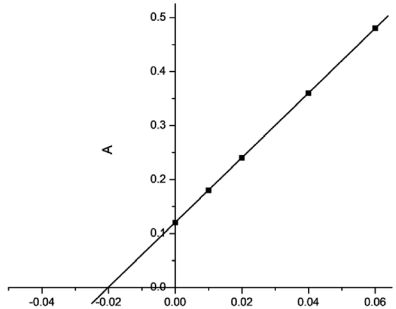 CPb adicionada (mg/L)
CPb adicionada (mg/L) Com base nos resultados, o teor de chumbo da amostra de tequila analisada é:
NaOH sólido; ácido acético (HAc) 2,00 mol L-1 (pKa = 4,74); ácido fosfórico (H3PO4) 2,00 mol L-1 (pKa1 = 2,23; pKa2 = 7,21; pKa3 = 12,32); amônia (NH3) 1,00 mol L-1 (pKa = 9,25); KH2PO4 sólido.
A mistura de quais dos reagentes acima, nas proporções adequadas, possibilita a preparação do tampão de pH 7,5, com boa capacidade de resistir às alterações de pH?
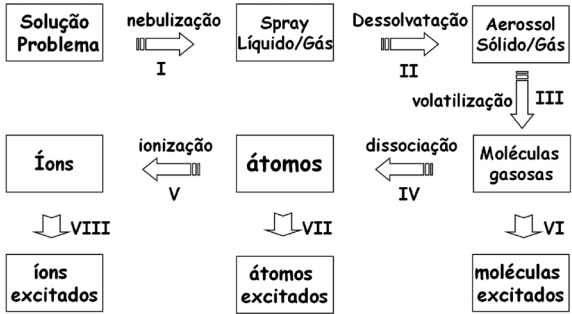
Considere o esquema e as seguintes afirmações:
I – A etapa IV é a responsável por produzir os átomos gasosos no estado fundamental. II – Na absorção atômica, utiliza-se um modulador, após a lâmpada, para eliminar os problemas que podem ser causados pela etapa VII. III – Somente a etapa V diminui a população de átomos gasosos no estado fundamental. IV – A etapa VII é indesejável para a absorção atômica, por diminuir a população de átomos gasosos no estado fundamental, porém é uma etapa essencial da espectrometria de emissão atômica.
Em relação a essas afirmativas, estão CORRETAS