Questões de Concurso
Comentadas para fundepes
Foram encontradas 1.146 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
PENSAR É TRANSGREDIR
Não lembro em que momento percebi que viver deveria ser uma permanente reinvenção de nós mesmos – para não morrermos soterrados na poeira da banalidade embora pareça que ainda estamos vivos.
Mas compreendi, num lampejo: então é isso, então é assim. Apesar dos medos, convém não ser demais fútil nem demais acomodada. Algumas vezes é preciso pegar o touro pelos chifres, mergulhar para depois ver o que acontece: porque a vida não tem de ser sorvida como uma taça que se esvazia, mas como o jarro que se renova a cada gole bebido.
Para reinventar-se é preciso pensar: isso aprendi muito cedo.
Apalpar, no nevoeiro de quem somos, algo que pareça uma essência: isso, mais ou menos, sou eu. Isso é o que eu queria ser, acredito ser, quero me tornar ou já fui. Muita inquietação por baixo das águas do cotidiano. Mais cômodo seria ficar com o travesseiro sobre a cabeça e adotar o lema reconfortante: “Parar pra pensar, nem pensar! ”
[...]
LUFT, Lya. Pensar é transgredir. Rio de Janeiro: Record, 2005. p. 21.
Disponível em: <http://pensador.uol.com.br/frase/MjgzMzA0/>. Acesso em: 23 set. 2016.
No segundo parágrafo, a conjunção “mas”, que inicia o período, exerce uma função importante na estrutura textual, pois estabelece relação de sentido (oposição ou contraste) entre dois enunciados. Isso significa dizer que a autora
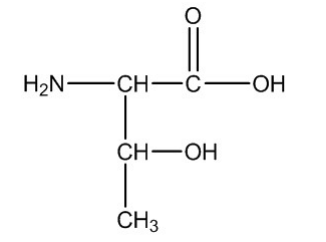
O nome, segundo a IUPAC, desse composto é
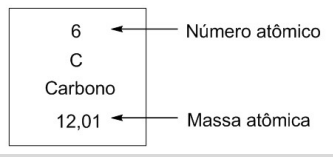
Essa diferença de massa atômica para o carbono pode ser atribuída à
Dado: massa molar do NaOH = 40 g/mol.
O composto em questão e o tratamento utilizado antes de seu descarte são, respectivamente,
De acordo com essas informações, assinale a alternativa que é um exemplo de mistura química.
Sobre o átomo de carbono do ponto de vista da TLV, assinale a alternativa correta.
Qual das alternativas descreve corretamente o que ocorre durante essa reação?
Dados: C = 12,01; H = 1,01; Br = 79,91
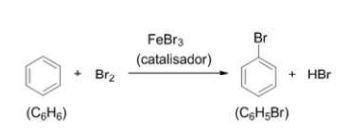
Determine o rendimento teórico do bromo-benzeno, quando 30 g de benzeno reage com 65 g de bromo.
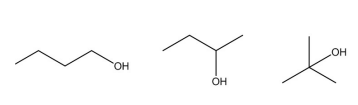
Dadas as afirmativas relacionadas a propriedades dos três isômeros do butanol da figura,
I. O 1-butanol apresenta o maior ponto de ebulição dentre os três compostos acima.
II. O 2-butanol apresenta o menor ponto de ebulição dentre os três compostos acima.
III. O 2-metil-2-propanol é o composto mais polar dessa série.
IV. O 1-butanol é o composto menos polar dessa série.
verifica-se que está/ão correta/s
O nome da vidraria usada e a concentração da solução de NaOH são, respectivamente,
Assinale a alternativa que apresenta a massa molecular (em u) do gás fétido liberado nessa reação. Dados da massa atômica em u: C = 12,01 u; H = 1,01 u; S = 32,07 u; O = 16,00 u; N = 14,01 u; Cl = 35,45 u.
Considerando-se o exposto, assinale a alternativa correta.
Assinale a alternativa que apresenta a reação balanceada corretamente.
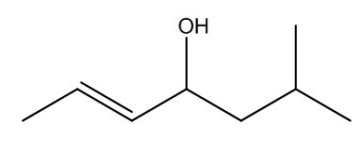
De acordo com a nomenclatura preconizada pela IUPAC, o nome desse composto é
Sobre essa técnica, assinale a alternativa correta.
Referente a esse reagente B, pode-se dizer que se trata de um reagente
NaCl(s) + AgNO3(s) → NaNO3(s) + AgCl(s)
Essa reação é classificada como