Questões de Concurso Para ufsm
Foram encontradas 1.656 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Para a determinação colorimétrica de um composto "X" na faixa de concentração de 1 a 8 mg/L, um analista realizou a medida de absorvância para 4 padrões em um colorímetro de bancada. A curva de calibração preparada pelo analista pode ser visualizada na figura.
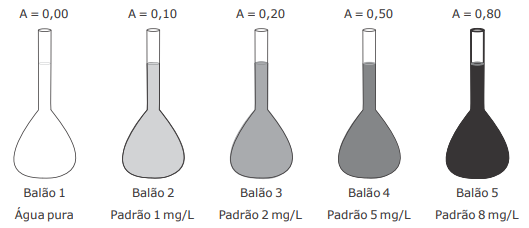
Sabendo que a análise do composto "X" deve apresentar absorvância no intervalo entre 0,10 e 0,80 e que o
rótulo da amostra contendo o composto "X" indica uma concentração de 2000 mg/L, considere as afirmativas
a seguir.
I - A amostra precisa ser diluída 100 vezes para que possa ser medida pelo método colorimétrico proposto no intervalo de concentração e absorvâncias mostrado na figura.
II - 1 mL da amostra deve ser pipetado em um balão volumétrico de 500 mL e o volume aferido com água desionizada, para que essa amostra possa ser medida pelo método colorimétrico proposto no intervalo de concentração e absorvâncias mostrado na figura.
III - 5 mL da amostra devem ser pipetados em um balão volumétrico de 500 mL e o volume aferido com água desionizada, para que essa amostra possa ser medida pelo método colorimétrico proposto no intervalo de concentração e absorvâncias mostrado na figura.
IV - 1 mL da amostra deve ser pipetado em um balão volumétrico de 250 mL e o volume aferido com água desionizada, para que essa amostra possa ser medida pelo método colorimétrico proposto no intervalo de concentração e absorvâncias mostrado na figura.
Está(ão) correta(s)
I - A absortividade molar de um composto aumenta com a sua concentração.
II - A absorvância e a absortividade molar do composto são inversamente proporcionais.
III - As dimensões do percurso ótico utilizado no colorímetro influenciam diretamente na quantidade de luz absorvida pelo composto.
IV - A absorvância medida para o composto de concentração "X" duplica, se a sua concentração passar para "4X" na medida colorimétrica com um percurso ótico de igual dimensão.
Está(ão) correta(s)
A precisão e a exatidão das medidas de um método analítico são fundamentais para a garantia da qualidade dos resultados obtidos. Medidas inexatas em um laboratório podem acarretar erros de interpretação de um determinado fenômeno, perda de produção na indústria, tratamentos equivocados e desperdício de energia em diversos setores produtivos e na sociedade. Portanto, todo método analítico deve apresentar um grau minimanente aceitável de precisão e exatidão dos resultados. Para isso, análises comparativas entre métodos independentes e análises de materiais de referência certificados devem ser realizadas para determinação desses parâmetros a partir dos resultados experimentais.
A figura a seguir ilustra quatro situações hipotéticas que podem acontecer nos resultados de medição por um determinado método analítico.
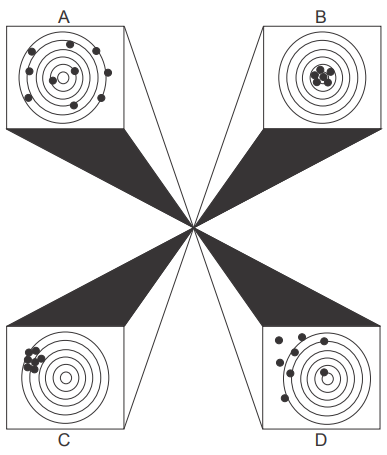
Fonte: Cienfuegos, Freddy. Estatística aplicada ao laboratório:
Rio de Janeiro: Interciência, 2005. p.7. (Adaptado)
Nesta figura, o centro do alvo simboliza o resultado esperado para as medidas repetidas em relação ao certificado de referência da amostra analisada. De acordo com essa definição, assinale V (verdadeiro) ou F (falso) em cada afirmativa a seguir.
( ) Na situação A os resultados são imprecisos.
( ) Na situação B os resultados são inexatos.
( ) Na situação C os resultados são precisos, mas inexatos.
( ) Na situação D os resultados são imprecisos, mas exatos.
A sequência correta é
SOLUÇÃO 1 - 10 mL da solução estoque (2,010 mol/L) foi pipetado e transferido para um balão volumétrico de 100 mL, onde o volume foi completado com água desionizada.
SOLUÇÃO 2 - 5 mL da SOLUÇÃO 1 foi pipetado e transferido para um balão volumétrico de 50 mL, onde o volume foi completado com água desionizada.
As concentrações finais da SOLUÇÃO 1 e SOLUÇÃO 2 são, respectivamente,
O cloreto de prata (AgCl) é um sal pouco solúvel em água pura, com um produto de solubilidade (Kps) igual a 1,8x10-10. Quando em contato com a água, apresenta uma baixa concentração de íons Ag+(1,34x10-5 mol/L) e íons Cl- (1,34x10-5 mol/L) no equilíbrio químico em solução devido à reação
AgCl(s) ⇄ Ag+ (aq) + Cl- (aq)
Em qual das soluções a seguir o sal AgCl será mais
insolúvel, quando comparado com a água pura?