Questões de Concurso
Para uerr
Foram encontradas 1.306 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
De acordo com o protocolo de Segurança na Prescrição, Uso e Administração de Medicamentos do Programa Nacional de Segurança do Paciente (PNSP- 2013), É necessário atender alguns itens de verificação para administração segura de medicamentos.
Marque a alternativa que contempla corretamente todos os “certos” para administrar medicação.
I. A ressonância magnética nuclear é a técnica mais importante para a elucidação estrutural de uma molécula e permite a detecção de muitos núcleos, tais como 1H, 13C, 15N, 29Si e 31P.
II. Os espectros de RMN de 13C geralmente são realizados com desacoplamento do núcleo de 1H.
III. A absorção da radiação faz com que o spin nuclear se alinhe ou gire em direção à maior energia. Após absorver energia, os núcleos remeterão radiação de radiofrequência (RF) e voltarão ao estado de energia mais baixo. Deste modo, para que os núcleos desenvolvam estados de energia necessários para que ocorra a absorção, o analito precisa ser colocado em um campo magnético intenso.
Assinale a alternativa correta.
O espectro abaixo foi obtido por espectroscopia UV-Visível.
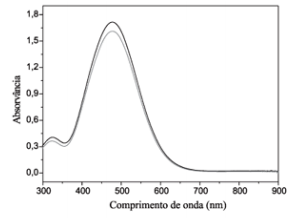
Assinale a alternativa correta que apresenta a
solução e o comprimento de onda máximo
(λmáx), respectivamente, que correspondem ao
espectrograma apresentado acima.
I. Separar a linha espectral de interesse das outras linhas emitidas pela fonte de radiação, através da utilização de um prisma ou rede de difração associado a duas fendas estreitas que servem para entrada e saída da radiação.
II. Através da fenda de saída, é possível decompor o feixe de radiação em discretos comprimentos de onda, com diferentes ângulos.
Assinale a alternativa correta.
I. O princípio fundamental da espectrometria de absorção atômica envolve a medida da absorção da intensidade da radiação eletromagnética, proveniente de uma fonte de radiação primária, por átomos gasoso no estado fundamental.
II. Os átomos excitados no atomizador retornam ao estado fundamental emitindo o mesmo comprimento de onda que é emitido pela fonte de radiação, mas um artifício eletrônico, denominado de modulação, permite que o detector detecte, idealmente, somente a radiação proveniente de radiação.
III. Os componentes básicos de um espectrômetro incluem fonte de radiação, sistema de atomização, conjunto monocromador, detector e processador.
Assinale a alternativa correta.
Em relação às reações orgânicas, resolva as etapas a seguir:
Etapa 1 – Substituir os hidrogênios dos carbonos insaturados do hexen-2-eno por radicais etila.
Etapa 2 – Submeter a substância buteno a uma reação de hidrogenação catalítica.
Etapa 3 – Submeter a substância resultante da etapa 2 a uma reação de monocloração.
Considere as afirmativas a seguir.
I. A substância resultante da etapa 1 é o 3-etil3-metil-hexano.
II. A substância obtida na etapa 2 é um hidrocarboneto de cadeia insaturada.
III. As substâncias resultantes das etapas 1 e 2 são isômeros de função.
IV. Na etapa 3, átomo de cloro substituirá preferencialmente o hidrogênio do carbono primário.
Assinale a alternativa correta.
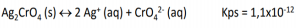
I. Eletroquímica é o estudo das reações químicas nas quais partículas carregadas (íons ou elétrons) atravessam a interface entre duas fases da matéria, tipicamente uma fase metálica (o eletrodo) e uma fase líquida de solução condutora, ou eletrólito.
II. Processos de oxidação e redução estão envolvidos no estudo da eletroquímica, onde as reações químicas ocorrem com o envolvimento de transferência de elétrons de um reagente para outro. Os dois processos não devem ocorrem simultaneamente e podem coexistir independentemente.
III. Lítio metálico é um agente redutor forte e se oxida facilmente. Pode-se dizer que ele é um agente oxidante fraco e se reduz com muita dificuldade. O lítio tem sido muito utilizado em baterias ou pilhas.
Assinale a alternativa correta.
C6 H12O6(s)⇾ 2C2 H5 OH (l) + 2CO2 (g)
Analise as seguintes sentenças:
I. Os açúcares são carboidratos com fórmula geral CnH2nOn, onde n é um número inteiro que dita o tamanho da molécula. Um dos açúcares mais importantes que existe é a glicose. II. Culturas ricas em carboidratos, como a cana, a mandioca, a beterraba e o milho, entre outras, são as melhores para a produção de etanol por via fermentativa. III. O processo fermentativo ocorre com a intervenção de enzimas presentes nos microorganismos. Enzimas são catalisadores biológicos específicos, que atuam no metabolismo celular.
Assinale a alternativa correta.
A figura abaixo apresenta a fórmula molecular de um composto encontrado no extrato de jasmim. Assinale a alternativa correta que contém a nomenclatura e família deste composto, respectivamente.
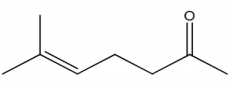
I. Moléculas orgânicas somente com ligação simples e elétrons σ, mas sem elétrons π ou elétrons não ligantes (n), tendem a não absorver na região do espectro UV-Visível.
II. Cromóforo é a parte da molécula que absorve a luz na região UV-Visível.
III. Hidrocarbonetos saturados podem ser medidos por espectroscopia UV-Visível.
Assinale a alternativa correta.
I. O Teste de Eber é utilizado para identificar a presença de decomposição em produtos de origem animal, como farinha de carne, farinha de peixe, farinha de ossos, entre outros. II. Para medir a rancidez hidrolítica das gorduras e avaliar a presença de ácidos graxos livres nos alimentos, utiliza-se a reação de Kreis. III. O Teste de peróxido é usado para medir o teor de gossipol no farelo de algodão ou na semente. É considerado baixo o índice menor que 0,04%.
Assinale a alternativa correta.