Questões de Concurso
Foram encontradas 8.674 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
I. A água utilizada para preparar soluções de base deve ser livre de dióxido de carbono.
II. Quando a água utilizada no preparo da base é supersaturada com o dióxido de carbono, ela deve ser congelada brevemente para eliminar o gás.
III. Um frasco de polietileno, tampado firmemente, pode fornecer a curto prazo uma proteção adequada contra a absorção de dióxido de carbono atmosférico por soluções padrão de base.
IV. Depois de longos períodos de armazenagem, as soluções de hidróxido de sódio tornam os frascos de polietileno quebradiços.
V. Soluções de hidróxido de sódio podem diminuir a concentração quando estocados em recipientes de vidro.
Sobre as afirmativas acima, pode-se declarar que está CORRETO o que está contido em
a ordem de ponto de ebulição é:
I. Extração por solvente
II. Destilação
( ) Requer energia térmica.
( ) Indicada quando os componentes a serem separados possuem a mesma volatilidade.
( ) Indicada quando os componentes são termicamente instáveis.
( ) Utiliza as diferenças de pressão de vapor dos componentes da mistura para efetuar a separação.
( ) A diferença de solubilidade dos componentes é fator determinante na separação.
Assinale a sequência CORRETA que preenche os parênteses de cima para baixo:
Dados os seguintes valores de massas molares (g/mol): CaCO3: 100; HCl: 36,5; NaOH: 40.
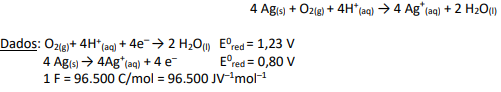
O valor da variação de energia livre, ∆G0 e a espontaneidade da reação é:
I. A velocidade de uma reação depende da concentração, mas a constante de velocidade não depende dela.
II. Quanto mais baixa for a energia de ativação, mais lenta a reação.
III. Se a velocidade de aparecimento de O2(g), 2 O3(g) → 3 O2(g), é 9 x 10–4 mol/L em determinado instante, a velocidade de desaparecimento do O3(g) é 18 x 10–4 mol/L.
Está correto o que se afirma em
I. Na reação química As2S3 + HNO3 + H2O → H3AsO4 + H2SO4 + NO, o nitrogênio sofre redução.
II. Na reação Cl2(g) + NaOH(aq) → NaCl(aq) + NaClO(aq) + H2O(l), o cloro sofre, ao mesmo tempo, oxidação e redução, tratando-se, nesse caso, de uma reação de auto-oxirredução.
III. Na equação química MnO4- + Fe2+(aq) + H+ (aq) → Mn2+(aq) + H2O + Fe3+(aq), a soma dos menores valores inteiros dos coeficientes estequiométricos é 24.
Está correto o que se afirma em
I. Na eletrólise do sulfato de sódio, a água é mais facilmente oxidada no ânodo do que o SO4- e no catodo as moléculas de água são reduzidas mais facilmente que os íons sódio.
II. Na eletrólise do cloreto de sódio fundido, pode-se obter Cl2(g) no ânodo.
III. Na eletrólise de uma solução aquosa de NaF, o F– será reduzido.
Está correto o que se afirma em
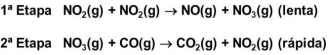
I. O intermediário NO3(g) é produzido lentamente na etapa 1 e é imediatamente consumido na etapa 2.
II. A lei de velocidade da reação é V = K [NO2]2 .
III. A etapa 2 é muito mais rápida que a etapa 1, isto é K2>>K1.
Está correto o que se afirma em
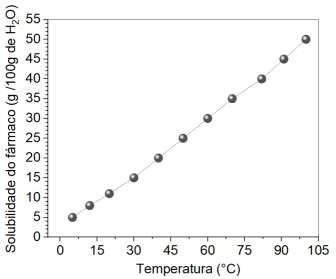
Se o químico optar por trabalhar com 40 g de água a 60°C, a quantidade máxima da substância que será dissolvida é:
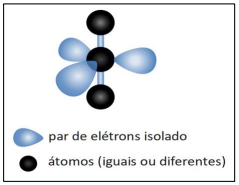
Sobre os conceitos de ligações covalentes e geometria molecular, assinale, a seguir, uma molécula que evidencia a configuração eletrônica espacial descrita.