Questões de Concurso
Foram encontradas 9.182 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Frasco 1: Formação de um precipitado branco com a adição de solução de cloreto de bário, sendo este, precipitado insolúvel em solução diluída de hidróxido de amônio, e também, insolúvel em solução diluída de ácido clorídrico. Frasco 2: Formação de um precipitado branco com a adição de solução de cloreto de sódio, sendo este precipitado solúvel em solução diluída de hidróxido de amônio. Frasco 3: Formação de precipitado amarelo com a adição de solução diluída de cromato de potássio. Frasco 4: Efervescência em contato com solução diluída de ácido clorídrico.
A partir dos resultados dos testes realizados pode-se inferir que o conteúdo de cada frasco é, respectivamente:
I. A Teoria Atômica de Dalton trouxe o átomo do campo filosófico para uma perspectiva científica. II. A descoberta dos raios catódicos foi fundamental para a conclusão de que a matéria é formada por partículas eletricamente carregadas. III. A estabilidade do modelo atômico de Rutherford poderia ser explicada pelas leis da Física Clássica, mas não pela Física de Planck-Einstein. IV. O efeito fotoelétrico observado por Einstein corroborou a idéia da dualidade onda-partícula dos elétrons.
Estão corretas apenas as afirmativas:
ICℓ(g) + H2(g) → HI(g) + HCℓ(g) (etapa lenta) ICℓ(g) + HI(g) → I2(g) + HCℓ(g) (etapa rápida)
Tendo em vista os referidos dados e sabendo-se que as concentrações molares das substâncias envolvidas estão representadas entre colchetes, pode-se afirmar corretamente que a equação de velocidade desta reação deverá ser representada por:
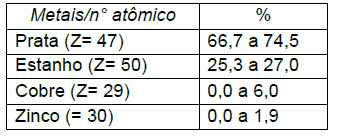
Roberto R. da Silva, et al. A química e a conservação dos dentes, Quím. Nov. na Esc.; N° 13, maio 2001.
Em relação aos metais presentes nas ligas e a tabela periódica é CORRETO a firmar:
Ca5(PO4 )3OH(s) 5Ca2+ (aq) + 3 PO4 3– (aq) + OH– (aq)
Esse processo é normal e ocorre naturalmente. O processo inverso, a mineralização, também é normal.
Roberto R. da Silva, et al. A química e a conservação dos dentes, Quím. Nov. na Esc.; N° 13, maio 2001.
Sobre a reversibilidade do equilíbrio, representado pela equação, através dos processos direto e inverso. Podemos concluir que esse equilíbrio é:
O local deve ser higienizado e esterilizado antes do início da pesagem. O responsável pelo procedimento deve obrigatoriamente realizar a assepsia das mãos e antebraços e usar uniforme de uso exclusivo na área analítica. A pesagem deve ser realizada o mais rápido possível para que a umidade não interfira na massa final da amostra.
Nessa situação hipotética, para preparar 1,5 mL de uma solução diluída a 10 μg/L diretamente a partir da solução-padrão estoque, é necessário tomar
10 μL da solução concentrada.
O amostrador de Kemmerer é indicado para análises microbiológicas, biológicas e químicas de águas altamente poluídas. Antes da coleta, esse equipamento deve ser autoclavado e lavado com água pura.
A técnica de refrigeração é a mais indicada para preservação de amostras para análises microbiológicas e determinações químicas, pois mantém a completa integridade de todos os parâmetros a serem analisados.
Quando a coleta da amostra for feita manualmente, a água deve ser coletada em contracorrente, ou seja, com a boca do frasco apontada para montante, a qual deve ser vedada rapidamente após a coleta. Outra opção igualmente correta de coleta consiste em mergulhar o frasco na água com a boca para baixo.
Os diversos componentes presentes na água, que alteram seu grau de pureza, podem ser retratados em termos de suas características físicas, químicas e biológicas. Essas características podem ser traduzidas na forma de parâmetros de qualidade da água. Acerca desse assunto, julgue o item seguinte.
Alcalinidade é a concentração de cátions multimetálicos em
solução, como os divalentes Ca2+ e Mg2+.
Os diversos componentes presentes na água, que alteram seu grau de pureza, podem ser retratados em termos de suas características físicas, químicas e biológicas. Essas características podem ser traduzidas na forma de parâmetros de qualidade da água. Acerca desse assunto, julgue o item seguinte.
O pH das águas naturais depende da presença de substâncias
dissolvidas que possuam propriedades ácido-básicas, e o seu
valor sofre influência da dissolução de rochas, da absorção de
gases da atmosfera, da oxidação da matéria orgânica e da
fotossíntese.
Com relação aos usos e à poluição das águas, julgue o item a seguir.
As atividades antropogênicas contribuem para a introdução de
compostos na água, afetando sua qualidade.
Acerca das características de qualidade da água, julgue o item subsequente.
Em contato com a água, materiais sólidos podem se dissolver
ou permanecer sólidos em suspensão ou no estado coloidal. No
estado coloidal, encontram-se algas, vírus, bactérias, matéria
orgânica e corantes vegetais, mas não argilas, siltes, areias e
sílicas, que só são encontradas em suspensão.
A respeito das propriedades da água, julgue os item que se segue.
A água tem seu volume reduzido e sua densidade
aumentada continuamente quando a temperatura é reduzida
de 25 ºC a 0 ºC.
A respeito das propriedades da água, julgue o item que se segue.
A água é uma das poucas substâncias que podem ser
encontradas na natureza nos estados sólido, líquido e gasoso.
Julgue o próximo item, relativos ao uso de equipamentos de proteção aplicados à segurança no laboratório.
Além do manuseio de líquidos voláteis, os procedimentos que
produzem poeira ou aerossóis devem ser realizados em capela
de exaustão.
Julgue o próximo item, relativos ao uso de equipamentos de proteção aplicados à segurança no laboratório.
Quando for necessário o uso de jaleco, este deve ser de mangas
curtas para evitar que respingos fiquem retidos no tecido das
mangas e possa causar alergia à pele.