Questões de Concurso
Foram encontradas 8.712 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
O ácido monoprótico, representado por HX, é misturado com excesso de Ba(OH)2 , reagindo segundo a equação abaixo.

Foram obtidos 15,00 g do produto BaX2 que foram quantitativamente reagidos com exatamente 59,00 mL de uma solução aquosa de ácido sulfúrico 1,00 mol L-1 , como mostrado na equação abaixo.
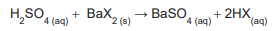
A partir dos dados do experimento, calculou-se a massa
molar de HX, em g mol -1
, e concluiu-se que era de 
Analista I: 59%; 61%; 63% Analista II: 64%; 65%; 66% Analista III: 43%; 43%; 43%
Nesse caso, conclui-se que
Um volume de 1,00 mL de um adoçante líquido à base de sacarina sódica (representada por SacNa) foi colocado num Erlenmeyer, onde também se adicionou 100 mL de água pura. A sacarina sódica reagiu exatamente com 22,00 mL de uma solução padronizada de AgNO3 (0,500 mol L-1 ) para precipitar quantitativamente a sacarina, conforme equação abaixo. No resultado, já se considerou a correção do branco.
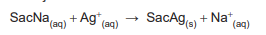
A concentração de sacarina, em g mL-1
, no adoçante, é
mais próxima de
Um analista precisou de 5,00 g de uma amostra de liga metálica e, usando uma balança de três casas decimais, nivelada e previamente calibrada, mediu um valor igual a 5,002 g.
O analista não fez a correção do ar, deslocado acima do prato da balança, pois o erro relativo, em %, decorrente da massa
de ar deslocado, em relação à massa da amostra, foi insignificante e mais próximo de
As substâncias orgânicas abaixo, quando em soluções aquosas, são sensíveis à condição ácida do meio, produzindo mudanças que afetam a capacidade de absorver radiação no espectro eletromagnético na região do visível. Por conta disso, são usadas como indicadores ácido-base, sendo eles: (P) fenolftaleína, (Q) vermelho de metila e (R) azul de bromotimol.
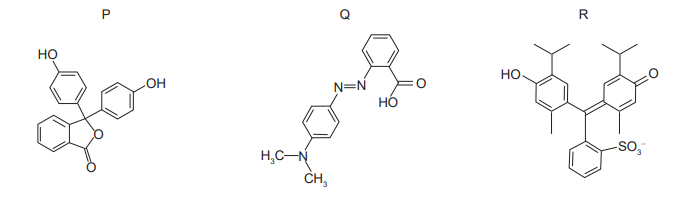
Sobre a funções orgânicas presentes nessas substâncias, conclui-se que
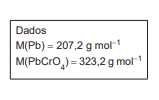
O íon chumbo pode ser determinado por gravimetria, na forma de cromato de chumbo (PbCrO4(s)), usando agente de
precipitação homogênea. Isso é alcançado pela adição de excesso de cloreto de cromo (III), que produz o íon cromato ao
ser oxidado pelo bromato (BrO3 -), também adicionado em excesso. A sequência resumida de reações é indicada abaixo:
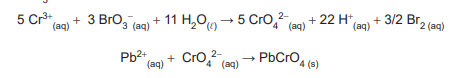
Uma alíquota de 60,000 g de resíduo foi totalmente dissolvido e submetido ao procedimento analítico gravimétrico em questão. A massa de 12,542 g de precipitado (após secagem até massa constante) foi obtida.
A percentagem (m/m) de chumbo presente na amostra foi de
Uma massa de 0,0575 g de um sal foi medida em balança, foi dissolvida em água e transferida para um balão volumétrico, onde o volume final foi ajustado para 25,00 mL.
Considerando as devidas precisões dos aparatos e respeitando os algarismos significativos, a concentração, em g L -1 , da solução é
A hidrazina se decompõe em gás nitrogênio e gás hidrogênio, segundo a equação abaixo.
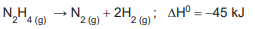
Em relação à sua vizinhança, ao decompor e formar produtos, esse sistema reacional
A decomposição da água é representada na reação termoquímica abaixo.
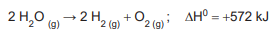
A variação de entalpia, em kJ, de formação de 1 mol de
H2
O(g) será de
O teor de mercúrio em um padrão certificado de água é 1,46 mg L-1 . Uma análise, com três réplicas, foi realizada, e os resultados obtidos, em mg L-1 , foram: 1,50, 1,52 e 1,54.
Sendo assim, o erro relativo da análise, em %, e o maior desvio obtido, em mg L-1 , são, respectivamente:
Um técnico possui quatro tipos de placas de metal (de cobre, de zinco, de chumbo e de prata) e soluções aquosas de sulfato de cobre, de sulfato de zinco, de nitrato de chumbo e de nitrato de prata.
Uma reação química redox espontânea ocorre quando a
placa de 
O tipo de risco, ao qual um indivíduo estará exposto ao manusear um produto químico, é indicado no pictograma usado nas rotulagens. A partir dos pictogramas, o usuário é alertado para os cuidados que devem ser tomados, a fim de se evitarem acidentes. Considere que, no rótulo de um frasco, onde há uma determinada substância química, está o pictograma representado a seguir.

Esse pictograma indica que a substância é
Para a realização de uma análise, é necessário o preparo
de uma solução tampão básica. Estão disponíveis os seguintes reagentes:
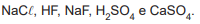
Os reagentes a serem selecionados para o preparo da solução tampão são:
Deseja-se preparar 800 mL de solução aquosa de hidróxido de sódio com pH igual a 12 e a 25 °C.
Assumindo-se completa dissociação do hidróxido de sódio em solução, a massa de base necessária para o preparo da solução, em g, corresponde a
Em um experimento, avaliou-se a seguinte reação química:

As concentrações iniciais de SO2 e O2 foram 0,3 mol/L e 0,2 mol/L, respectivamente. No início da reação, não havia SO3 no reator, mas atingido o equilíbrio, sua concentração foi igual a 0,2 mol/L.
Para esse sistema, a constante de equilíbrio, em termos
de concentrações, é igual a
Em um laboratório, estão disponíveis os seguintes sais:
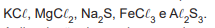
A dissolução de um desses sais em água acarretou a formação de uma solução aquosa com pH ácido.
O sal dissolvido correspondeu a
Em um estudo avaliou-se a velocidade da seguinte reação química:
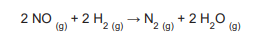
Foram realizados três experimentos distintos, nos quais se variaram as concentrações iniciais dos reagentes, conforme apresentado na Tabela a seguir.
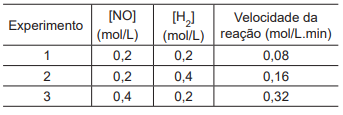
A constante cinética dessa reação química, em L2 mol-2
min-1
,
é igual a
Uma solução aquosa de cloreto de sódio foi preparada e teve suas temperaturas de ebulição e de congelamento determinadas sob pressão de 1 atm.
Ao se interpretarem os resultados obtidos, conclui-se que a solução salina apresenta:
Em uma prática de laboratório, 1 L de solução aquosa foi obtido ao se misturar 600 mL de solução 0,010 mol/L de cloreto férrico e 400 mL de solução 0,020 mol/L de cloreto de cálcio.
Admitindo-se completa dissociação dos sais, a concentração de íons cloreto na mistura formada, em mol/L, é igual a
Ácido sulfúrico em excesso foi adicionado a uma amostra de 150 g de alumínio metálico impuro, verificando-se a formação de 10 g de H2 , após a completa reação do alumínio.
Admitindo-se que as impurezas presentes não reagiram
com o ácido, o grau de pureza do alumínio é igual a