Questões de Concurso
Foram encontradas 8.674 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!

*elemento e informações fictícias.
Com base nos dados apresentados, a massa atômica que representa o Eterium é:
Na matriz energética nacional, a participação das fontes fósseis passou de 9% em 2000, para 14% em 2020. O crescimento se dá, principalmente, por dois fatores: aumento da demanda por energia, que não foi acompanhada pela oferta, e as repetidas crises hídricas no país.
(Adaptado de CNN, 02/07/2022)
Com relação às transformações de energia e às termoelétricas, analise os itens a seguir:
I. O combustível usado em uma usina termelétrica a gás natural é renovável, pois o biogás usado é oriundo da fermentação do lixo orgânico.
II. Em uma usina termoelétrica a gás natural, as transformações de energia são de química para térmica, desta para energia cinética e, por fim, para energia elétrica.
III. A energia não pode ser destruída, embora possa ser criada e transformada.
Está correto o que se afirma em
A imagem a seguir mostra o cromatograma obtido ao final do experimento e a linha representa o local onde as amostras das tintas das canetas foram colocadas inicialmente.

A cromatografia apresenta: uma fase estacionária, no caso desse experimento, o papel; e uma fase móvel, um líquido ou gás, que nesse experimento é a água.
No experimento citado, a mistura que contém pigmentos insolúveis na fase móvel da cromatografia é a
O experimento serviu para demonstrar a ocorrência de um fenômeno
A equação química abaixo representa a síntese do íon triiodeto.
S2 O82- (aq) + 3 I- (aq) → 2 SO42- (aq) + I3 - (aq)
A fim de descobrir a ordem da reação, três experimentos foram realizados, e os resultados encontrados estão na tabela a seguir. Analise os dados da tabela e assinale a alternativa que possui a ordem desta reação.
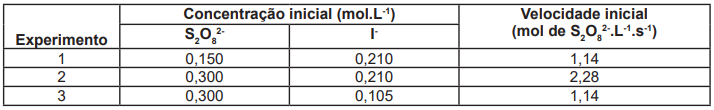
Fonte: ATKINS, P.; JONES, L.; LAVERMAN, L. Princípios de Química: Questionando a vida moderna e o meio ambiente. 7. ed. Porto Alegre: Bookman, 2018. p.191.
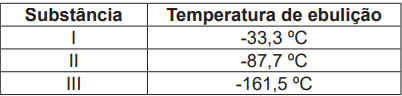
Considerando a relação existente entre as interações intermoleculares e a temperatura de ebulição, e comparando a temperatura de ebulição das três substâncias, assinale a alternativa que identifica, corretamente, a fórmula química das substâncias I, II e III. São dados os números atômicos dos elementos químicos H (Z=1), C (Z=6), N (Z=7) e P (Z=15).
Frasco A: REAÇÃO A : H2(g) + I2(g) ⇌ 2HI(g)
Frasco B: REAÇÃO B: 2NO2(g) ⇌ 2NO(g) + O2(g)
Considere os gases como ideias.
Se o volume de cada frasco for reduzido para um terço do volume inicial, é possível observar que:
TOMA, Henrique Eisi. Ligação Química: Abordagem clássica ou quântica? Química Nova na Escola, n. 6, p. 8-12, 1997.
A tabela a seguir correlaciona os valores de Energia de Ionização (EI) e Afinidade Eletrônica (AE) para dois diferentes elementos químicos, denominados X e Y. A partir desses dados, assinale a alternativa correta em relação à possibilidade de ligação química formada entre elementos:

LEE, J. D. Química Inorgânica não tão concisa. 5. ed. São Paulo: Editora Blucher, 1999. LANG, Peter F.; SMITH, Barry C. Ionization energies of atoms and atomic ions. Journal of chemical education, v. 80, n. 8, p. 938, 2003.
O átomo é um sistema eletronicamente neutro, onde o número de prótons é igual ao número de elétrons. A distribuição dos elétrons faz-se por divisão em sete camadas ao redor do núcleo: K, L, M, N, O, P, Q.
Fonseca, Albino. Ciências, 9° ano. 3. ed. São Paulo: IBEP, 2013
Quanto às soluções, julgue o item seguinte.
Ocorre uma reação de precipitação quando iodeto de chumbo (PbI2) e nitrato de potássio (KNO3) reagem formando nitrato de chumbo (Pb(NO3)2) e iodeto de potássio (KI) sólidos, através da equação apresentada a seguir.
PbI2 (aq) + 2 KNO3 (aq) → Pb(NO3)2 (s) + 2 KI (s)
Quanto às soluções, julgue o item seguinte.
Um composto molecular dissolve‑se em água
formando, invariavelmente, moléculas carregadas
eletricamente (íons) dispersas pela solução, formando
um eletrólito.
Quanto às soluções, julgue o item seguinte.
Quando em solução aquosa, os íons positivos
provenientes de um sólido iônico (cátions) são atraídos
pelo lado negativo da molécula da água, enquanto os
íons negativos (ânions) são atraídos pelo lado positivo.
Considerando os cálculos estequiométricos e os assuntos correlatos, julgue o item a seguir.
Conforme a equação genérica a seguir, a soma dos valores representados pelas letras minúsculas a + b deve ser igual à soma dos valores representados pelas letras minúsculas c + d:
a A (g) + b B (g) → c C (g) + d D (g)
Considerando os cálculos estequiométricos e os assuntos correlatos, julgue o item a seguir.
Em uma reação química, os coeficientes
estequiométricos mostram que os átomos podem ser
criados ou destruídos em uma reação balanceada.
A respeito dos ácidos, bases, sais e óxidos, julgue o item seguinte.
Os óxidos iônicos binários são compostos formados
por oxigênio e por mais dois outros elementos
químicos, sendo sua fórmula apresentada por esses
elementos precedidos pelo símbolo do oxigênio.
A respeito dos ácidos, bases, sais e óxidos, julgue o item seguinte.
O cloreto de sódio, de fórmula mínima NaCl, é um
retículo unidimensional, cujas moléculas iônicas
compactadas representam a relação existente entre
os íons presentes na estrutura, como entidade isolada
nessa composição.
Em relação às ligações químicas, julgue o item a seguir.
A ligação química entre os metais é o resultado do
baixo empacotamento observado entre os átomos
que formam a estrutura metálica, o que resulta na
característica de baixa condutividade elétrica.