Questões de Concurso
Foram encontradas 8.680 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Com relação às mudanças de estado físico da matéria e à calorimetria, julgue o item subsequente.
As mudanças de estado de líquido para gasoso podem ser
corretamente chamadas de evaporação, ebulição e calefação,
as quais se diferenciam principalmente pela velocidade em
que ocorrem.
Julgue o próximo item, relativo a propriedades dos hidrocarbonetos.
O estado de agregação de hidrocarbonetos (sólido, líquido ou
gasoso) está relacionado diretamente com a quantidade de
carbonos em suas cadeias, as quais, quando compostas por
mais de dezessete carbonos, resultam em substâncias no
estado sólido nas condições normais de temperatura e
pressão.
Julgue o próximo item, relativo a propriedades dos hidrocarbonetos.
Hidrocarbonetos são compostos insolúveis em água, por
serem praticamente polares, unidos por dipolo induzido.
Considerando que a estequiometria tem base em leis ponderais e compreende cálculos e regras para determinar a correta proporção das substâncias que se pretende utilizar, julgue o item a seguir.
A lei de Lavoisier, também conhecida como lei das
proporções constantes, tem como base o princípio de que a
soma das massas reagentes em um recipiente fechado é igual
à soma das massas dos produtos da reação.
Considerando que a estequiometria tem base em leis ponderais e compreende cálculos e regras para determinar a correta proporção das substâncias que se pretende utilizar, julgue o item a seguir.
Os coeficientes estequiométricos em uma reação química
podem ser determinados por tentativas; nesse caso, a fim de
melhorar a assertividade, são utilizadas algumas regras
empíricas, por exemplo, aquela em que se balanceiam, por
último, o carbono, o hidrogênio e o oxigênio, nessa ordem.
4 Au(minério) + 8 NaCN(aq) + O2(g) + 2 H2O(l) → 4 Na[Au(CN)2](aq) + 4 NaOH(aq)
A espécie química solúvel [Au(CN)2]− é posteriormente imobilizada sobre carvão ativado, e o ouro é recuperado por redução eletroquímica:
[Au(CN)2]−(aq) + e− → Au(s) + 2 CN−(aq)
Dados: Massa molar (g mol−1): Au = 197, NaCN = 49.
Considerando a estequiometria das reações, qual é a massa de ouro que se espera extrair, utilizando-se 1 kg de cianeto de sódio?
H2PO3F(aq) + 2 NaOH(aq) → Na2PO3F(aq) + 2 H2O(l)
Adicionou-se uma solução de NaOH 0,14 mol L-1 ao ácido até ser obtido 0,28 mol de Na2PO3F. Qual foi o volume da solução de NaOH adicionado?
A química orgânica e as características do carbono
Começou com a síntese da Ureia, A Química Orgânica que conhecemos; Com alguns grupos funcionais, E as propriedades que sabemos, E seu grande brilhantismo, Voltando-se para a pesquisa científica Que, independentemente do organismo, Descreveu um resultado inesperado, Contrariando a teoria do Vitalismo. (...) Compostos que ficaram conhecidos Como isômeros, para explicar O fenômeno isomeria é que dois Ou mais compostos venham apresentar. Diferente fórmula estrutural E mesma fórmula molecular
SOUSA, Mario Marques de. A Literatura de Cordel no Ensino de Química: uma Proposta Didática. In: Anais do 20º Encontro Nacional de Ensino de Química (ENEQ Pernambuco). Anais...Recife(PE) UFRPE/UFPE, 2020. Disponível em: http//www.even3.com.br/anais/ENEQPE2020.
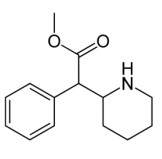
Sabendo que a isomeria abrange boa parte dos estudos relacionados à Química Orgânica, assinale a alternativa que apresenta uma característica atribuída aos isômeros.
Considerando a estrutura química apresentada, assinale a alternativa correta.
Qual a quantidade de água, em mL, que deverá ser adicionada para que a concentração do soluto seja reduzida para 0,04 mol/L?
Identifique abaixo as afirmativas verdadeiras ( V ) e as falsas ( F ) com base nessas informações.
( ) A adição de mais água na solução saturada favorecerá a solubilização do sal, o que acarretará a diminuição da massa do precipitado.
( ) Se uma quantidade de solução saturada for retirada, ocorrerá um aumento da massa do precipitado.
( ) O aumento da temperatura favorecerá a solubilização do sal, o que caracteriza um processo endotérmico.
( ) Se a solução permanecer aberta e exposta ao ar, ocorrerá diminuição da massa de sal precipitado.
( ) A dissolução do sal em um líquido é sempre um processo exotérmico.
Assinale a alternativa que indica a sequência correta, de cima para baixo.
Na sequência, efetuou-se a filtração e o sólido não dissolvido foi separado e, depois de seco, medida a massa resultante.
A solubilidade do Ag2SO4 em água é 2,0×10–2 mol/L e sua massa molar é aproximadamente 312 g/mol.
Assinale a alternativa que indica corretamente a quantidade, em gramas, de sulfato de prata obtida após a filtração.
No gráfico abaixo estão representados os caminhos de uma reação com catalisador e uma sem catalisador.
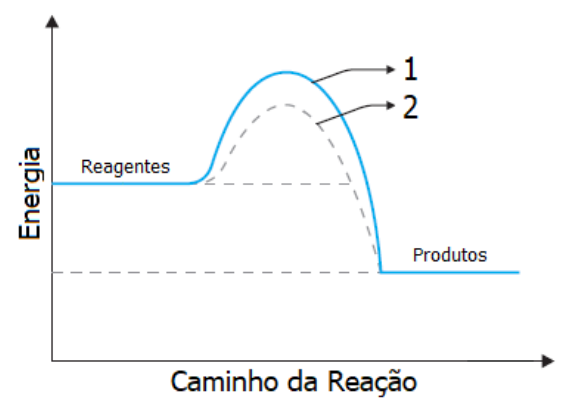
Identifique abaixo as afirmativas verdadeiras ( V ) e as falsas ( F ) com base nesse gráfico.
( ) A curva 1 refere-se à reação não catalisada e a curva 2 refere-se à reação catalisada.
( ) A energia de ativação da curva 1 é maior do que a da curva 2.
( ) A utilização de um catalisador na reação aumenta o valor de ∆H.
( ) O complexo ativado da curva 1 apresenta a mesma energia do complexo ativado da curva 2.
( ) Se a reação seguir o caminho da curva 2, ela será mais rápida.
Assinale a alternativa que indica a sequência correta,
de cima para baixo.
CuS + HNO3 ➔ Cu(NO3)2 + S + NO + H2O
Identifique abaixo as afirmativas verdadeiras ( V ) e as falsas ( F ) em relação à reação dada.
Assinale a alternativa que indica a sequência correta, de cima para baixo.
( ) A soma total de íons entre os produtos deve ser igual à soma total de íons entre os reagentes.
( ) O agente oxidante é o HNO3 e o agente redutor é o CuS.
( ) O total de elétrons cedidos pelo agente redutor deve ser igual ao total de elétrons recebidos pelo agente oxidante.
( ) Os coeficientes 3, 8, 3, 3, 2, 4 tornarão a equação balanceada.
Observe a equação abaixo: 3 MnO2 + KClO3 + 6 KOH ➔ 3 K2MnO4 + KCl + 3 H2O
Analise as afirmativas abaixo em relação ao assunto.
Analise as afirmativas abaixo em relação ao assunto.
1. O “Mn” do dióxido de manganês perdeu elétrons.
2. A soma dos índices mínimos inteiros é igual a 16.
3. MnO2 é o agente redutor e KClO3 é o agente oxidante.
4. O “K” do clorato de potássio não perdeu e nem ganhou elétrons.
Assinale a alternativa que indica todas as afirmativas corretas.
Nesse caso, assinale a alternativa que indica corretamente o que deve ser realizado.
A reação de eletrólise é classificada como: