Questões de Concurso
Foram encontradas 3.145 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
3 Fe2O3(s) → 2 Fe3O4(s) + 1/2 O2(g)
A porcentagem de Fe e a porcentagem de Fe3O4 presentes na amostra, são respectiva e aproximadamente:
Dados: Fe = 55,847 g/mol; Fe2O3 = 159,69 g/mol Fe3O4 = 231,54 g/mol
( ) Ao aquecer um tubo de ensaio contendo qualquer substância, recomenda-se voltar a extremidade aberta para si mesmo e nunca para uma pessoa próxima. ( ) As substâncias que chegarem a ser usadas nunca devem ser retornadas para o frasco de onde foram tiradas. ( ) Sempre que proceder à diluição de um ácido concentrado, é recomendado adicionar lentamente, sob constante agitação, a água sobre o ácido. ( ) É recomendado verificar cuidadosamente o rótulo do frasco que contém o dado reagente, antes de tirar dele qualquer porção do seu conteúdo.
Assinale a sequência correta.
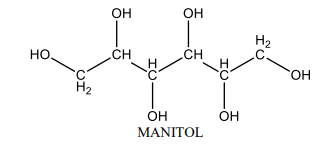
Observando a estrutura do manitol, percebe-se que essas moléculas têm facilidade de formar um gel com óleo diesel devido ao fato de
P2O5(S) + 9 H2O(I) → 2PO43- (aq) + 6 H3O+(I)
2 PO43-(aq) + 6 Ag+(aq) → 2 Ag3PO4(S)
Ag+(aq) + SCN-(aq) → AgSCN(s)
Sendo assim, a porcentagem de P2O5 presente na amostra é, aproximadamente, igual a:
Dados: Massas molares em g/Mol C = 12,01 N = 14,00; O = 16,00; P = 30,97; S = 32,06; Ag = 107,87
Observe as equações abaixo.
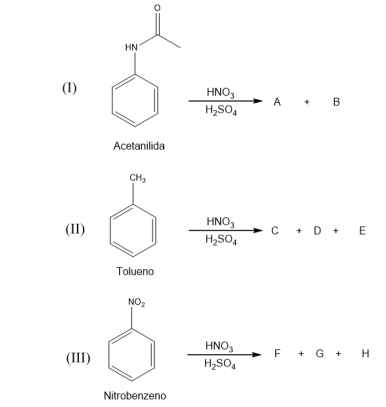
Sobre essas equações, marque V para as afirmativas verdadeiras e F para as falsas.
( ) Na equação (I), os produtos A e B serão a p-nitroacetanilida e a m-nitroacelanilida, respectivamente, sendo o primeiro produto em maior quantidade. ( ) Na equação (II), os produtos C, D e E serão o o-nitrotolueno, p-nitrotolueno e m-nitrotolueno, respectivamente, sendo o terceiro produto em menor quantidade. ( ) Na equação (III), os produtos F, G e H serão o-dinitrobenzeno, p-dinitrobenzeno e m-dinitrobenzeno, respectivamente, sendo o terceiro produto em maior quantidade.
( ) Nas equações (I) e (II), os substituintes dos anéis aromáticos dos reagentes possuem o mesmo efeito.
Assinale a sequência correta.
Considere a seguinte reação de substituição:
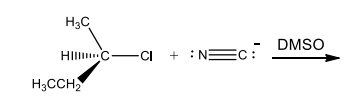
Dados: Números Atômicos (Z)
H = 1; C = 6; N = 7; Cl = 17
Sobre essa reação, é correto afirmar:
1- Compostos de Pt(II) e Pt(IV) ( ) Úlceras Gástricas
2- Compostos de Au(I) ( ) Malária
3- Salicilatos de Bismuto(III) ( ) Tumores diversos
4- Compostos de Li(I) 5- Ferroquina ( ) Transtorno de humor
Marque a sequência correta.
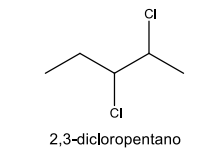
O número máximo de estereoisômeros que podem existir para essa molécula é:
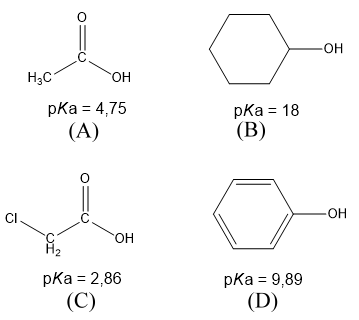
Sobre o tema, marque V para as afirmativas verdadeiras e F para as falsas.
( ) Comparando os compostos (B) e (D), o composto (D) é mais ácido devido à distribuição de carga elétrica, fazendo o oxigênio do grupo -OH ficar mais positivo, portanto o próton é mantido com uma força menor. ( ) Em uma reação de (D) com NaHCO3 aquoso, ocorre a remoção de um próton do composto (D), formando um produto derivado de (D) solúvel em água. ( ) A maior acidez do composto (D) quando comparada à do (B) pode ser atribuída às estruturas dos híbridos de ressonância daquele composto apresentarem cargas nas posições meta em relação à hidroxila, tornando o oxigênio mais positivo. ( ) O composto (C) é mais ácido do que (A) devido ao efeito substituinte provocado pelo átomo de Cl.
Assinale a sequência correta.
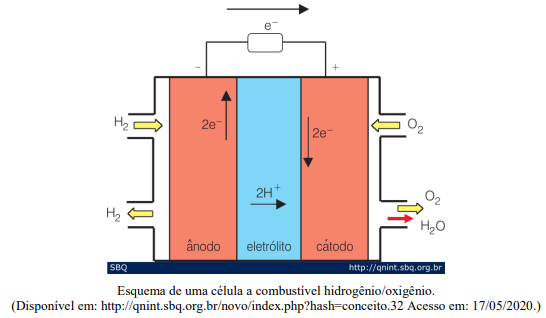
Levando em consideração o funcionamento de uma célula a combustível esquematizado acima, marque V para as afirmativas verdadeiras e F para as falsas.
( ) As células a combustível são células galvânicas nas quais a energia de Gibbs de uma reação química é transformada em energia elétrica (por meio da geração de uma corrente). ( ) A principal semelhança em relação às pilhas e baterias é o fato de, nas células a combustível, os reagentes já estarem armazenados no interior do sistema. ( ) Devido à dificuldade de se armazenar H2, uma alternativa para alimentação das células a combustível é o metanol, que, por sua vez, apresenta a desvantagem de gerar CO e/ou CO2 que são gases de efeito estufa. ( ) O combustível é reduzido de forma contínua no ânodo, enquanto oxigênio é oxidado no cátodo, produzindo água como produto final e energia elétrica.
Assinale a sequência correta.
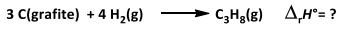
Observe as reações a seguir:
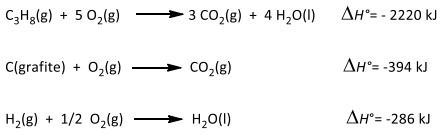
De acordo com as reações acima e os dados fornecidos, o valor da entalpia padrão de formação do gás propano, em quilojoules, é igual a:
( ) As quatro moléculas possuem o mesmo número de domínios ligantes. ( ) A molécula SF4 possui geometria molecular de gangorra e a BrF5 possui geometria piramidal quadrada. ( ) A molécula do ClF3 tem a geometria na forma de T. ( ) A molécula do XeF2 tem geometria de gangorra.
Dados: Números Atômicos (Z)
F = 9; S = 16; Cl = 17; Br = 35; Xe = 54
Assinale a sequência correta.
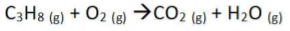
O balanceamento da equação é dado pelos coeficientes estequiométricos, nesta ordem:
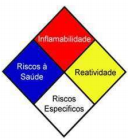
Em cada uma das cores, exceto branco, é utilizada uma escala de zero (0 - substância sem risco) a quatro (4 - risco sério ou grave). Para o losango branco, utilizam-se códigos para riscos específicos, como OXI (oxidante), ACID (ácido),
 (reage com
água de maneira perigosa) etc.
(reage com
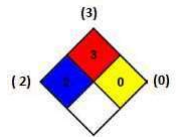
água de maneira perigosa) etc. A substância que apresenta o diagrama de Hommel abaixo é
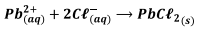
Admite-se que os íons Pb2+ foram consumidos em sua totalidade formando cloreto de chumbo(Il). O excesso de ácido é titulado com solução 0,1 mol.L-1 de hidróxido de sódio (NaOH), consumindo 30mL da base.
O teor (em base mássica) de ions Pb2+ na amostra de efluente, expresso em porcentagem, é aproximadamente iguala:
[Ma(u): Pb = 207; Cl 35,5; Na=23;0=16;H=1]
Um técnico coletou uma alíquota de 200mL dessa última solução e adicionou 600mL de solução aquosa de NaCl 0,5 mol.L-1. A concentração de K2CO3, em mol.L-1, na solução salina preparada pelo técnico corresponde a:
[Ma(u): K = 39; Cl 35,5; Na = 23; 0= 16; C = 12]