Questões de Concurso
Para ifc-sc
Foram encontradas 2.058 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
I. Nas linhas 07 e 09, o emprego das aspas deve-se ao emprego de uma citação empregada fora de seu sentido original. II. Na linha 07, as duas vírgulas separam um adjunto adverbial intercalado. III. Na linha 15, o emprego dos dois pontos se deve à introdução de uma explicação sobre o termo “alguns”.
Quais estão corretas?
A 4 Day Week Global (1) também irá avaliar o impacto (2) da redução (3) de jornada (4) na Vockan (5).
I. O sistema de escalas visava à busca por uma operação eficiente com funcionários trabalhando mais horas.
II. O processo de início da nova jornada de trabalho foi gradativo.
III. Para o executivo da Vockan, a nova jornada trará ganhos tanto na produtividade quanto na manutenção de um quadro de funcionários de qualidade.
Quais estão corretas?

No que se refere à cromatografia líquida, julgue as afirmativas abaixo:
I. O aumento da polaridade da fase móvel causa uma redução nos tempos de retenção na cromatografia em fase normal e um aumento nos tempos de retenção na cromatografia em fase reversa.
II. Na cromatografia de fase reversa, o analito mais
polar elui depois do analito menos polar.
III. O tempo morto (tempo de retenção da fase móvel)
é o tempo necessário para que um soluto retido
passe através de uma coluna cromatográfica.
IV. A equação de van Deemter descreve a eficiência
cromatográfica, levando em consideração os
efeitos de múltiplos caminhos, da difusão
longitudinal e de transferência de massa.
Assinale a alternativa que apresenta a resposta correta:

A respeito da técnica de eletroforese capilar, analise as seguintes afirmativas: I. O uso de um capilar possibilita a dissipação do calor gerado pela passagem da corrente elétrica. II. A mobilidade eletroforética é diretamente proporcional ao coeficiente de atrito e inversamente proporcional à carga do íon. III. Na separação de espécies com caráter ácidobase, a mobilidade eletroforética dependerá do pH do eletrólito empregado na análise. IV. As amostras podem ser introduzidas por injeção hidrodinâmica ou eletrocinética.
Assinale a alternativa que apresenta a resposta correta:
I. O atomizador em chama é o mais adequado para inserção de amostras sólidas. II. Os espectros de absorção atômica são constituídos por um número ilimitado de linhas espectrais largas. III. A função do monocromador é dispersar a radiação nos comprimentos de onda que a compõe e selecionar uma faixa estreita de comprimentos de onda. IV. Em análises usando essa técnica, podem surgir interferências, como por exemplo, a interferência espectral, onde mais de um elemento pode absorver no mesmo comprimento de onda. Esse tipo de interferência pode ser eliminado selecionando comprimentos de onda diferentes.
Assinale a alternativa que apresenta a resposta correta:
No que se refere a essa técnica, analise os itens subsequentes:
I. O uso do plasma acoplado indutivamente em comparação à atomização em chama é mais vantajoso por se tratar de uma fonte de temperatura mais elevada, e, portanto o processo de atomização é mais completo, ocasionando aumento do sinal analítico. II. Um atomizador de chama proporciona maior sensibilidade que o forno de grafite, pois o tempo de residência do analito no caminho óptico é maior. III. O material do cátodo de uma lâmpada de cátodo oco independe da amostra analisada. IV. A sensibilidade da espectroscopia de absorção atômica é dependente da temperatura de atomização.
Assinale a alternativa que apresenta a resposta correta:
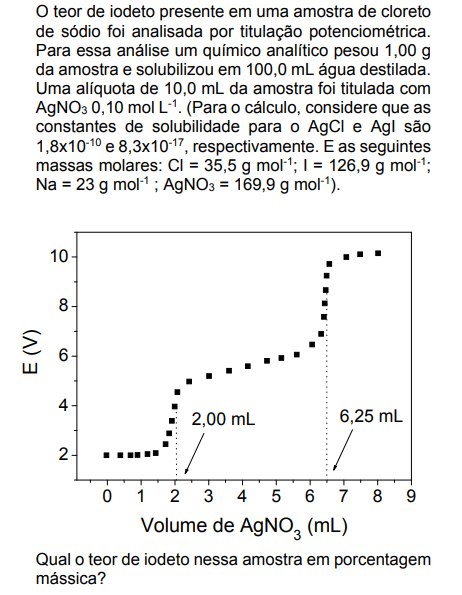




Assinale a alternativa que apresenta a resposta correta:

