Questões de Concurso
Para químico
Foram encontradas 3.476 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
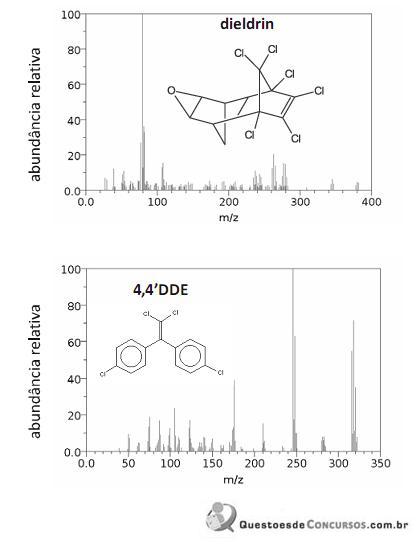
Os espectros de massa mostrados acima são, respectivamente, do dieldrin e do 4,4’DDE, compostos que usualmente têm seus picos parcialmente sobrepostos em cromatogramas. Considere, ainda, que o elemento cloro apresenta massa molar igual a 35,5 g/mol e apenas dois isótopos, com números de massa iguais a 35 e 37. A partir dessas informações, julgue os itens que se seguem.
A porcentagem do isótopo do cloro com número de massa 35 é maior que 70%.
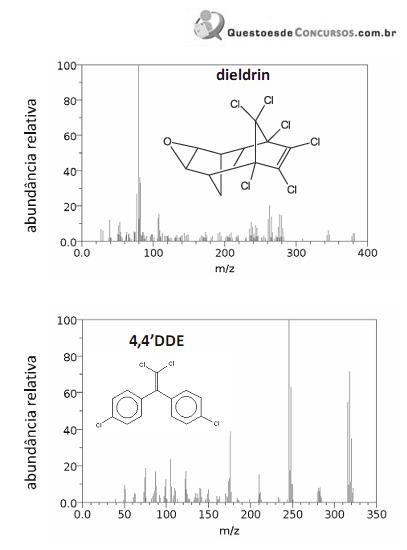
Os espectros de massa mostrados acima são, respectivamente, do dieldrin e do 4,4’DDE, compostos que usualmente têm seus picos parcialmente sobrepostos em cromatogramas. Considere, ainda, que o elemento cloro apresenta massa molar igual a 35,5 g/mol e apenas dois isótopos, com números de massa iguais a 35 e 37. A partir dessas informações, julgue os itens que se seguem.
No espectro de massa do 4,4’DDE, o pico em m/z igual a 116 corresponde a um íon molecular do composto.
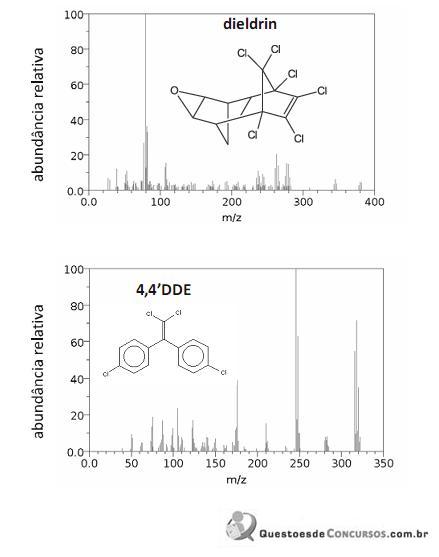
Os espectros de massa mostrados acima são, respectivamente, do dieldrin e do 4,4’DDE, compostos que usualmente têm seus picos parcialmente sobrepostos em cromatogramas. Considere, ainda, que o elemento cloro apresenta massa molar igual a 35,5 g/mol e apenas dois isótopos, com números de massa iguais a 35 e 37. A partir dessas informações, julgue os itens que se seguem.
Por meio dos espectros de massa dos compostos 4,4’DDE e dieldrin, demonstra-se que, em uma análise cromatográfica, mesmo que ocorra a sobreposição dos respectivos picos, caso se utilize a detecção por espectrometria de massa com monitoramento seletivo de íons, é possível separar as respostas dos dois componentes.
Considerando-se a fase estacionária da coluna utilizada, é correto afirmar que o composto correspondente ao pico 7 apresenta maior ponto de ebulição que o composto correspondente ao pico 1.
Considerando-se os dados fornecidos na tabela e que o fator de retenção para o lindano seja igual a 0,50, é correto afirmar que o fator de retenção para o composto aldrin é igual a 1,0.
Para se obter uma melhor resolução entre os picos 5 e 6, faz-se necessário empregar uma taxa mais elevada de aquecimento da coluna.
A análise cromatográfica da amostra acima pode ser realizada, sem prejuízos à identificação e à quantificação dos compostos, substituindo-se o detector por captura de elétrons por um detector por ionização em chama.
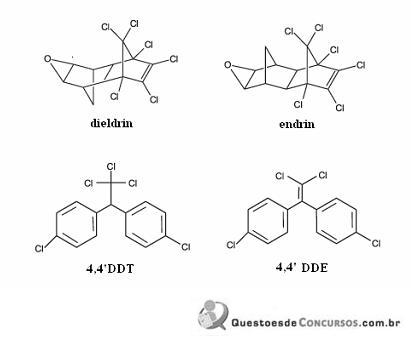
Considerando a figura acima, que ilustra as estruturas químicas de quatro pesticidas, julgue os itens que se seguem.
O dieldrin e o endrin são isômeros constitucionais.
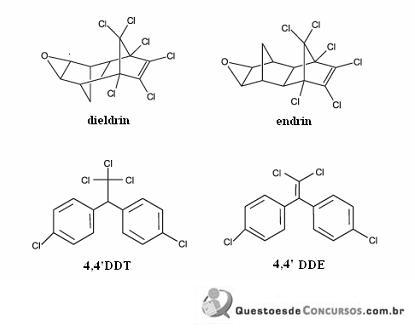
Considerando a figura acima, que ilustra as estruturas químicas de quatro pesticidas, julgue os itens que se seguem.
O composto 4,4’DDE denomina-se 1,1-di(p-clorobenzil)-eteno.
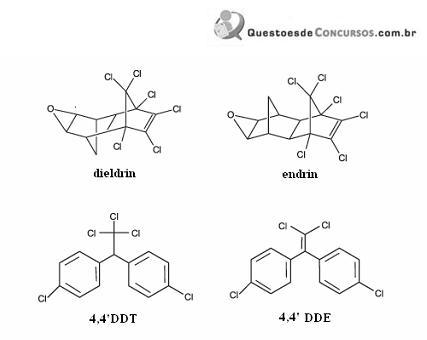
Considerando a figura acima, que ilustra as estruturas químicas de quatro pesticidas, julgue os itens que se seguem.
A molécula de dieldrin apresenta a função éter.
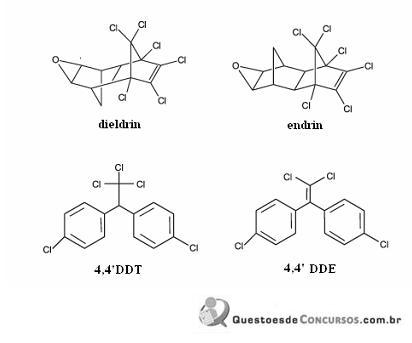
Considerando a figura acima, que ilustra as estruturas químicas de quatro pesticidas, julgue os itens que se seguem.
O composto 4,4’DDE consiste no principal produto da reação do 4,4’DDT com KOH, que se processa via mecanismo de eliminação bimolecular.
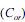 e na fase aquosa
e na fase aquosa 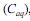 , quando atingido o
, quando atingido o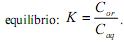
Dois estudantes realizaram a extração de um composto, a partir de uma solução aquosa com a concentração do composto igual a 0,0100 mol/L. O estudante A realizou uma única extração, utilizando 100 mL da solução aquosa e 100 mL de 1-octanol, e o estudante B utilizou o mesmo volume da solução aquosa, mas realizou duas extrações consecutivas, cada uma com 50 mL de 1-octanol.
Considerando o conjunto de informações apresentado acima e que o coeficiente de partição do composto no sistema 1-octanol/água seja igual a 2,0, julgue os itens que se seguem.
A fração do composto extraída pelo estudante B será maior que a extraída pelo estudante A.
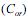 e na fase aquosa
e na fase aquosa 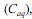 , quando atingido o
, quando atingido o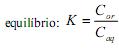
Dois estudantes realizaram a extração de um composto, a partir de uma solução aquosa com a concentração do composto igual a 0,0100 mol/L. O estudante A realizou uma única extração, utilizando 100 mL da solução aquosa e 100 mL de 1-octanol, e o estudante B utilizou o mesmo volume da solução aquosa, mas realizou duas extrações consecutivas, cada uma com 50 mL de 1-octanol.
Considerando o conjunto de informações apresentado acima e que o coeficiente de partição do composto no sistema 1-octanol/água seja igual a 2,0, julgue os itens que se seguem.
Considerando-se que o composto não sofra qualquer reação adicional nas fases aquosa e orgânica, é correto inferir que a porcentagem desse composto extraída pelo estudante A será maior que 80%.
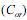 e na fase aquosa
e na fase aquosa 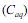 , quando atingido o
, quando atingido o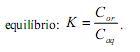
Dois estudantes realizaram a extração de um composto, a partir de uma solução aquosa com a concentração do composto igual a 0,0100 mol/L. O estudante A realizou uma única extração, utilizando 100 mL da solução aquosa e 100 mL de 1-octanol, e o estudante B utilizou o mesmo volume da solução aquosa, mas realizou duas extrações consecutivas, cada uma com 50 mL de 1-octanol.
Considerando o conjunto de informações apresentado acima e que o coeficiente de partição do composto no sistema 1-octanol/água seja igual a 2,0, julgue os itens que se seguem.
Caso o composto seja um ácido que sofra ionização em água, então, a fração extraída será tanto maior quanto mais elevado for o pH da fase aquosa.
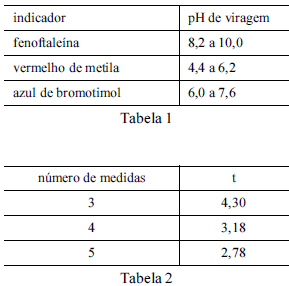
Considere que uma solução de NaOH foi padronizada por meio da titulação, em quadruplicata, com 20,00 mL de uma solução padrão de biftalato de potássio 0,1000 mol/L e que a concentração média encontrada para a solução de NaOH foi de 0,080 mol/L, com uma estimativa do desvio padrão de ±0,002 mol/L. Considere, ainda, a tabela 1, em que é apresentado o pH de viragem de alguns indicadores ácido-base, e a tabela 2, em que são apresentados os valores do parâmetro t de student para uma probabilidade de 95%.
Com base nessas informações, julgue os itens seguintes
Entre os indicadores apresentados na tabela 1, o mais
adequado à titulação em questão é o vermelho de metila.
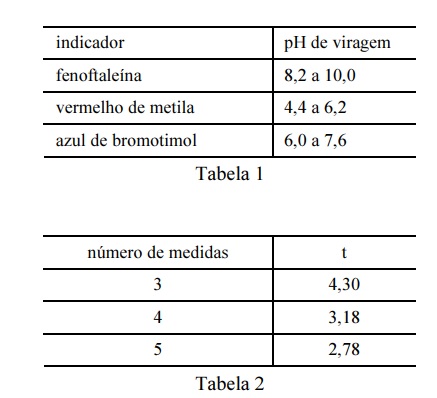
Considere que uma solução de NaOH foi padronizada por meio da titulação, em quadruplicata, com 20,00 mL de uma solução padrão de biftalato de potássio 0,1000 mol/L e que a concentração média encontrada para a solução de NaOH foi de 0,080 mol/L, com uma estimativa do desvio padrão de ±0,002 mol/L. Considere, ainda, a tabela 1, em que é apresentado o pH de viragem de alguns indicadores ácido-base, e a tabela 2, em que são apresentados os valores do parâmetro t de student para uma probabilidade de 95%.
Com base nessas informações, julgue os itens seguintes.
Considerando-se a inexistência de erros sistemáticos, é correto afirmar que a probabilidade de que o valor real da concentração de NaOH esteja no intervalo compreendido entre 0,078 e 0,082 será maior que 95%.

Considere que uma solução de NaOH foi padronizada por meio da titulação, em quadruplicata, com 20,00 mL de uma solução padrão de biftalato de potássio 0,1000 mol/L e que a concentração média encontrada para a solução de NaOH foi de 0,080 mol/L, com uma estimativa do desvio padrão de ±0,002 mol/L. Considere, ainda, a tabela 1, em que é apresentado o pH de viragem de alguns indicadores ácido-base, e a tabela 2, em que são apresentados os valores do parâmetro t de student para uma probabilidade de 95%. Com base nessas informações, julgue os itens seguintes.
A partir dos resultados obtidos, pode-se inferir que o volume
médio da solução de NaOH gasto na titulação é maior que
22,0 mL.
Preparou-se 100 mL de uma solução padrão de biftalato de potássio, de acordo com o seguinte procedimento: (i) pesagem de um béquer vazio em uma balança analítica; (ii) pesagem do béquer contendo 2,0000 g do biftalato na mesma balança; (iii) dissolução do biftalato, por meio da adição de água suficiente ao béquer; (iv) transferência de todo o conteúdo do béquer para um balão volumétrico de 100,00 mL; (v) preenchimento do balão com água até o menisco.
Considerando as informações acima e que os desvios padrão sejam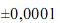 g, para uma simples leitura na balança utilizada, e
g, para uma simples leitura na balança utilizada, e 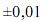 mL, para uma leitura de menisco no balão, julgue o próximo item.
mL, para uma leitura de menisco no balão, julgue o próximo item.
O desvio padrão relativo para a concentração da solução de biftalato de potássio preparada é maior que 1,0×10-4 .
Considerando as informações acima e que os desvios padrão sejam
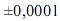 g, para uma simples leitura na balança utilizada,
g, para uma simples leitura na balança utilizada,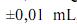 e , para uma leitura de menisco no balão, julgue os próximos itens.
e , para uma leitura de menisco no balão, julgue os próximos itens.Caso a solução de biftalato preparada seja usada, posteriormente, na padronização de uma solução básica, a presença de impurezas no biftalato usado para a preparação de sua solução gerará um erro aleatório que, consequentemente, afetará a precisão dos resultados obtidos durante a padronização.

Com base nessas informações, julgue os itens que se seguem.
Os complexos de metais de transição com configuração eletrônica d9 , tais como o complexo
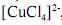 , caracterizam-se pela geometria quadrado planar.
, caracterizam-se pela geometria quadrado planar. 