Questões de Concurso
Para professor - química
Foram encontradas 4.164 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
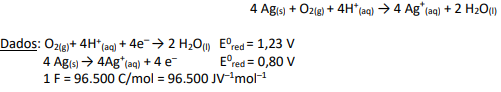
O valor da variação de energia livre, ∆G0 e a espontaneidade da reação é:
(CH3)3CBr + OH– → (CH3)3COH + Br–
Considerando os dados apresentados, a lei de velocidade para a reação é:
I. A velocidade de uma reação depende da concentração, mas a constante de velocidade não depende dela.
II. Quanto mais baixa for a energia de ativação, mais lenta a reação.
III. Se a velocidade de aparecimento de O2(g), 2 O3(g) → 3 O2(g), é 9 x 10–4 mol/L em determinado instante, a velocidade de desaparecimento do O3(g) é 18 x 10–4 mol/L.
Está correto o que se afirma em
I. Na reação química As2S3 + HNO3 + H2O → H3AsO4 + H2SO4 + NO, o nitrogênio sofre redução.
II. Na reação Cl2(g) + NaOH(aq) → NaCl(aq) + NaClO(aq) + H2O(l), o cloro sofre, ao mesmo tempo, oxidação e redução, tratando-se, nesse caso, de uma reação de auto-oxirredução.
III. Na equação química MnO4- + Fe2+(aq) + H+ (aq) → Mn2+(aq) + H2O + Fe3+(aq), a soma dos menores valores inteiros dos coeficientes estequiométricos é 24.
Está correto o que se afirma em
I. Na eletrólise do sulfato de sódio, a água é mais facilmente oxidada no ânodo do que o SO4- e no catodo as moléculas de água são reduzidas mais facilmente que os íons sódio.
II. Na eletrólise do cloreto de sódio fundido, pode-se obter Cl2(g) no ânodo.
III. Na eletrólise de uma solução aquosa de NaF, o F– será reduzido.
Está correto o que se afirma em