Questões de Concurso
Para pesquisador tecnologista em metrologia e qualidade - engenharia química
Foram encontradas 58 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
I. O gás de combustão é analisado para controle do processo em um equipamento conhecido como aparelho de orsat.
II. Independente dos possíveis mecanismos de reação, em termos de estequiometria, as reações são C + O2 → CO2, 4H + O2 → 2 H2O e S + O2 → SO2.
III. No equipamento, a amostra de gás é borbulhada em solução ligeiramente alcalina e analisada volumetricamente usando soluções de absorção.
Está(ão) correta(s) a(s) afirmativa(s)
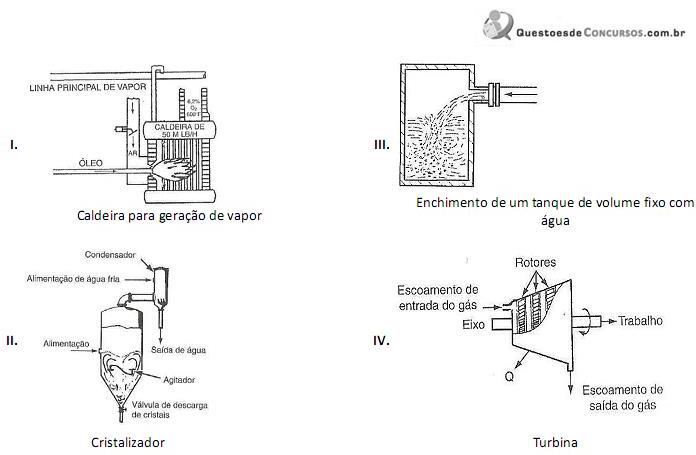
Estão corretos apenas os processos
I. As matérias-primas essenciais da fabricação moderna do ácido nítrico são o amoníaco anidro, o ar, a água e uma tela de platina-ródio como catalisador.
II. A reação 4 NH3(g) + 5 O2(g) → 4 NO(g) 6 H2O(g) éuma reação catalítica muito lenta, que se efetua pela passagem de amoníaco, através de uma tela muito fina.
III. O ácido é retirado da torre através de um coletor de ácido.
A imagem a seguir representa um diagrama Txy à pressão constante para um sistema binário exibindo o equilíbrio íquido / líquido / vapor (ELLV).
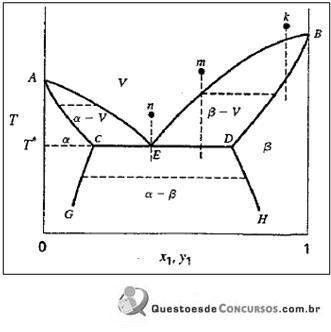
De acordo com as informações, marque V para as afirmativas verdadeiras e F para as falsas.
( ) Os pontos C e D representam as duas fases líquidas e o ponto E representa a fase vapor.
( ) Na temperatura acima T*, o sistema pode ser uma única fase líquida, duas fases
(líquida e vapor) ou uma única fase vapor dependendo da composição global.
( ) As composições das fases em equilíbrio e, consequentemente, a localização
das linhas não variam com a pressão.
( ) A região identificada por V existe fases líquidas e vapor em equilíbrio.
A sequência está correta em
I. A velocidade de reação é baseada na massa do catalisador sólido.
II. Operado em regime estacionário.
III. A forma diferencial do balanço molar é dFA/dW = r’A.
Está(ão) correta(s) a(s) afirmativa(s)