Questões de Concurso
Para técnico em química - médio
Foram encontradas 89 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Tendo como referência as informações precedentes, julgue o item subsecutivo, a respeito de fundamentos de estatística.
Se a determinação cromatográfica de isoctano em uma
mistura de hidrocarbonetos revelou a presença de 3,1943%
de isoctano, com desvio padrão de 0,0327%, então o
laudo de análise deve apresentar o resultado da seguinte
forma: (3,1943 ± 0,0327)%.
Tendo como referência as informações precedentes, julgue o item subsecutivo, a respeito de fundamentos de estatística.
Se uma determinada amostra de hidrocarbonetos analisada
pelo referido método apresenta um valor y igual
a 2,65 unidades arbitrárias, então a porcentagem molar de
isoctano nessa amostra é inferior a 1,5%
Tendo como referência as informações precedentes, julgue o item subsecutivo, a respeito de fundamentos de estatística.
No método dos mínimos quadrados, os valores calculados de
xi, yi, xi2
, yi2
, xiyi e seus respectivos somatórios devem ser
arredondados para três algarismos significativos antes de se
calcular os demais parâmetros da regressão linear.
Tendo como referência as informações precedentes, julgue o item subsecutivo, a respeito de fundamentos de estatística.
Se uma amostra de hidrocarbonetos contém 5% de isoctano
em quantidade de matéria analisada pelo método descrito,
então a área sob o pico cromatográfico do isoctano terá valor
superior a 10 unidades arbitrárias.
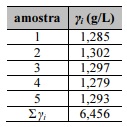
Com base nessas informações, julgue o próximo item.
A partir dos dados apresentados, infere-se que o coeficiente
de variação é superior a 0,008.

Com base nessas informações, julgue o próximo item.
A média amostral é superior a 1,290 g/L.
Acerca de controle metrológico de instrumentos, equipamentos e soluções, julgue o item subsequente.
Bombas de combustível em postos de gasolina são exemplos
de instrumentos sujeitos ao controle metrológico legal por
parte do INMETRO.
Acerca de controle metrológico de instrumentos, equipamentos e soluções, julgue o item subsequente.
Conforme a normatização do INMETRO, instrumentos de
medição devem ser fabricados de forma a ficarem isentos da
influência de fatores ambientais.
Acerca de controle metrológico de instrumentos, equipamentos e soluções, julgue o item subsequente.
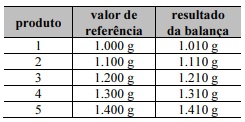
Se os dados na tabela a seguir correspondem a medidas de cinco produtos, feitas em uma mesma balança, e os respectivos valores de referência de cada produto, então essas medidas foram feitas com erro sistemático.
Em relação à análise instrumental, julgue o item a seguir.
A lei de Beer-Lambert relaciona a absorvância à
concentração do soluto e ao caminho óptico (espessura da
célula), valendo-se, para tanto, do coeficiente de absorção
molar (ou coeficiente de extinção molar).
Em relação à análise instrumental, julgue o item a seguir.
A espectroscopia UV-VIS baseia-se na medida da absorção,
pelas moléculas ou íons presentes na amostra, de radiação
eletromagnética na faixa de comprimento de onda entre
130 nm e 820 nm.
Em relação à análise instrumental, julgue o item a seguir.
Na cromatografia a líquido, os componentes de uma amostra
se distribuem em duas fases: uma estacionária e outra móvel,
e, com isso, são separados. Para tal, usa-se uma bomba de
alta pressão que empurra a fase móvel através de um
cilindro. O detector registra, de uma forma indireta, a
concentração dos componentes na fase móvel que passa
por ele.
Em relação à análise instrumental, julgue o item a seguir.
Na espectroscopia no infravermelho, são usados
espectrômetros tais como o de dispersão, que utiliza
interferência de ondas para obter o espectro, e o FTIR
(espectrômetro de infravermelho por transformada de
Fourier), que divide a radiação em diferentes comprimentos
de onda usando aproximações matemáticas.
Em relação à análise instrumental, julgue o item a seguir.
Na cromatografia a gás, a fase móvel é um gás inerte (como
hélio ou nitrogênio) e a fase estacionária é uma coluna com
revestimento especial. Via de regra, os componentes da
amostra são separados com base em suas interações com a
fase móvel.
Acerca de eletrodos de membrana de vidro, titulação potenciométrica e medida de condutividade, julgue o item subsequente.
A membrana de vidro em um eletrodo combinado é
fabricada a partir de um vidro especial de composição
controlada; esse vidro é uma mistura de sílica, barrilha ou
soda (carbonato de sódio) e calcário (carbonato de cálcio), o
que permite que a membrana responda especificamente à
concentração de íons H+
no intervalo de pH de 2 a 10.
Acerca de eletrodos de membrana de vidro, titulação potenciométrica e medida de condutividade, julgue o item subsequente.
Titulação potenciométrica é um método analítico utilizado
para determinar a concentração de uma substância em uma
solução com base na medição do potencial elétrico gerado
durante uma reação química.
Acerca de eletrodos de membrana de vidro, titulação potenciométrica e medida de condutividade, julgue o item subsequente.
A condutividade elétrica é uma propriedade que depende da
presença de íons dissolvidos em soluções iônicas, como
ácidos, bases e sais, pois os íons permitem a passagem da
corrente elétrica. A medida da condutividade é afetada pela
temperatura, geralmente decrescendo com o aumento da
temperatura.
Julgue o próximo item, a respeito da equação de Nernst e de potencial de eletrodo, eletrodos indicadores e medidas de pH.
Potencial de eletrodo é a medida do potencial individual de
um eletrodo reversível no estado-padrão, ou seja, solutos em
concentração de 1 mol/kg e gases à pressão de 1 bar, ambos
a 273 K.
Julgue o próximo item, a respeito da equação de Nernst e de potencial de eletrodo, eletrodos indicadores e medidas de pH.
O pH é uma medida que indica o grau de acidez,
neutralidade ou alcalinidade de uma solução e varia de 0 a
14: se o pH for menor que 7, a solução será ácida; acima de
7, será básica; e na faixa de 6 até 8, será neutra.
A partir das informações do texto precedente, julgue o próximo item.
Nos campos de produção, após a separação dos gases
presentes nas amostras de petróleo, água livre é removida
por decantação.