Questões de Concurso
Para patologia clínica
Foram encontradas 12.826 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
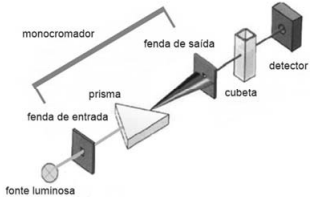
Considerando o esquema precedente, que representa os principais componentes de um espectrofotômetro, julgue o item a seguir.
Se a fonte luminosa estiver na região do ultravioleta, então é
correto empregar uma cubeta de vidro, já que o vidro
absorve a radiação ultravioleta.

Considerando o esquema precedente, que representa os principais componentes de um espectrofotômetro, julgue o item a seguir.
O detector serve para medir a diferença entre a luz absorvida
e a luz transmitida pela amostra.

Considerando o esquema precedente, que representa os principais componentes de um espectrofotômetro, julgue o item a seguir.
A cubeta é um recipiente transparente que contém a solução
a ser analisada; sobre ela incidirá a radiação selecionada.
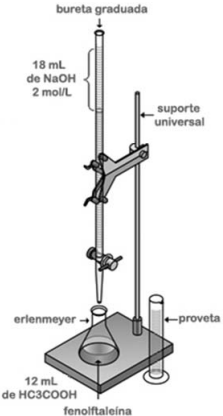
Tendo como referência a figura precedente, que representa uma titulação volumétrica, julgue o próximo item.
Entre as vidrarias empregadas em análises analíticas, a
bureta e a proveta são as que exibem o mais elevado grau de
precisão e exatidão, em comparação com o balão
volumétrico.
O Sistema Internacional de Unidades, também conhecido como SI, estabelece como as unidades de medida das grandezas físicas fundamentais e derivadas devem ser descritas na ciência. Contudo, no dia a dia, várias informações são amplamente divulgadas em outros sistemas. Nesse sentido, sabendo que 1 pol = 2,45 cm, 1 mL = 1 cm3 e que 1 W = 1 J/s, julgue o item que se segue.
De acordo com o SI, 1 h 5 min correspondem a 3.900 s.
O Sistema Internacional de Unidades, também conhecido como SI, estabelece como as unidades de medida das grandezas físicas fundamentais e derivadas devem ser descritas na ciência. Contudo, no dia a dia, várias informações são amplamente divulgadas em outros sistemas. Nesse sentido, sabendo que 1 pol = 2,45 cm, 1 mL = 1 cm3 e que 1 W = 1 J/s, julgue o item que se segue.
Se o consumo de energia residencial fosse medido no SI,
então um consumo de 300 kWh seria descrito com um
consumo de 300.000 J.
O Sistema Internacional de Unidades, também conhecido como SI, estabelece como as unidades de medida das grandezas físicas fundamentais e derivadas devem ser descritas na ciência. Contudo, no dia a dia, várias informações são amplamente divulgadas em outros sistemas. Nesse sentido, sabendo que 1 pol = 2,45 cm, 1 mL = 1 cm3 e que 1 W = 1 J/s, julgue o item que se segue.
Conforme o SI, o volume de uma caixa d’água de 500 L
corresponde a meio metro cúbico.
O Sistema Internacional de Unidades, também conhecido como SI, estabelece como as unidades de medida das grandezas físicas fundamentais e derivadas devem ser descritas na ciência. Contudo, no dia a dia, várias informações são amplamente divulgadas em outros sistemas. Nesse sentido, sabendo que 1 pol = 2,45 cm, 1 mL = 1 cm3 e que 1 W = 1 J/s, julgue o item que se segue.
Se o tamanho das telas de TV fosse medido no SI, então uma
TV de 50 pol seria descrita com uma TV de 2 m.
Embora as sensações térmicas de quente e frio sejam bastante relativas, é possível entender melhor a ideia de temperatura a partir da análise dos números obtidos nas escalas termométricas. Nesse sentido, considerando que os pontos fixos das escalas térmicas Fahrenheit e Celsius são (32 °F; 212 °F) e (0 °C; 100 °C), respectivamente, julgue o item seguinte.
Se a temperatura de um corpo for representada pelo mesmo
valor numérico nas escalas Fahrenheit e Celsius, então,
certamente, essa temperatura será negativa.
Embora as sensações térmicas de quente e frio sejam bastante relativas, é possível entender melhor a ideia de temperatura a partir da análise dos números obtidos nas escalas termométricas. Nesse sentido, considerando que os pontos fixos das escalas térmicas Fahrenheit e Celsius são (32 °F; 212 °F) e (0 °C; 100 °C), respectivamente, julgue o item seguinte.
Se um termômetro de mercúrio permite a medida de
temperatura nas escalas Fahrenheit e Celsius
simultaneamente, então o espaçamento entre duas marcas
consecutivas na escala Fahrenheit é certamente maior que na
escala Celsius.
Embora as sensações térmicas de quente e frio sejam bastante relativas, é possível entender melhor a ideia de temperatura a partir da análise dos números obtidos nas escalas termométricas. Nesse sentido, considerando que os pontos fixos das escalas térmicas Fahrenheit e Celsius são (32 °F; 212 °F) e (0 °C; 100 °C), respectivamente, julgue o item seguinte.
Se uma variação térmica de 5 °C sofrida por um objeto fosse
medida na escala Fahrenheit, então ela seria descrita como
uma variação térmica de 9 °F.
Se um paciente febril apresenta temperatura de 40 °C, então, em um termômetro graduado em Fahrenheit, esse paciente apresentará temperatura superior a 120 °F.



Acerca da eliminação de resíduos químicos, julgue o item a seguir.
Compostos orgânicos não halogenados com menos de
5 carbonos devem ser descartados na rede de esgoto.
Acerca da eliminação de resíduos químicos, julgue o item a seguir.
Substâncias oxidantes e redutoras devem ser juntamente
acondicionadas em frascos comuns para descarte.
Acerca da eliminação de resíduos químicos, julgue o item a seguir.
Soluções ácidas devem ser neutralizadas com hidróxidos ou
carbonatos antes de serem descartadas; o pH deve ser
ajustado entre 6 e 8 e, se necessário, um banho de gelo deve
ser utilizado durante a neutralização.
Acerca da eliminação de resíduos químicos, julgue o item a seguir.
Para o descarte de soluções de metais pesados, é indicada a
precipitação dos íons metálicos na forma de hidróxidos; em
alguns casos, a precipitação deve ser feita com sulfeto.