Questões de Concurso Sobre transformações químicas e energia em química
Foram encontradas 1.412 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
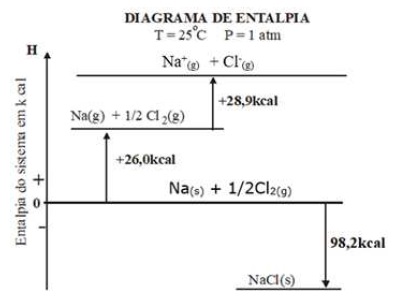
1 C4H10(g) + 6.5 O2(g) → 4 CO2(g) + 5 H2O(g)
Analisando a equação acima balanceada adequadamente e os dados de entalpiaspadrão de formação de cada um dos seus componentes (abaixo), assinale a alternativa que apresenta qual será o valor de ∆H (calor de reação), em Kcal, para a queima completa do butano Dados: entalpias-padrão de formação para 1mol da substância: 4 C(s) + 5 H2(g) → 1C4H10(g) ∆H = -125 Kcal; 1 C(s) + 1O2(g) → 1CO2(g) ∆H = -394 Kcal e 1 H2(g) + 0.5 O2(g) → 1 H2O(g) ∆H = -242 Kcal
A2 + B2 → 2 AB
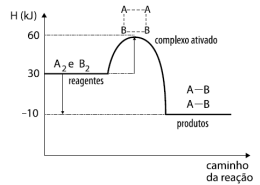
Disponível em: i_662d64349cafcb5b_html_55011cd1.png (463×350) (quimicaevestibular.com.br). Acesso em 27 de Julho de 2021.
Com relação ao gráfico acima, temos as seguintes afirmativas: I. A reação absorve calor; II. A energia de ativação da reação é 60 KJ; III. O valor da entalpia da reação (∆H) é de -40 KJ; IV. Ao colocarmos um catalisador na reação, diminuímos a sua entalpia (∆H), tornando-a mais rápida.
Estão corretas as afirmativas:
Adaptado. CÉLULA A COMBUSTÍVEL, COMO FUNCIONA – Autoentusiastas. Acesso em 20 de Julho de 2021.
A seguir, temos um esquema da célula a combustível de gás hidrogênio.
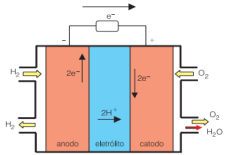
Esquema da célula a combustível de gás hidrogênio. Disponível em: www.usp.br/portalbiossistemas/?p=4316#:~:text=Em outras palavras%2C nessa célula a combustível a,célula a combustível é%3A H2 %2B ½O2→ H2O. Acesso em 20 de Julho de 2021.
A reação global balanceada da célula a combustível de gás hidrogênio é:
H2 (g) + ½O2 (g) → H2O (g)
Analisando o esquema da célula a combustível de gás hidrogênio (acima) e sua reação global balanceada, assinale a alternativa correta.
Adaptado. Pilhas e Baterias de Lítio. Pilha e Baterias de íon lítio (uol.com.br). (Acesso em 23 de Julho de 2021).
Com relação à pilha de lítio usada em marca-passos e as transformações nela ocorridas, assinale a alternativa correta.