Questões de Vestibular Comentadas sobre química
Foram encontradas 1.427 questões
Tabagismo passivo é a inalação da fumaça de derivados do tabaco, tais como cigarro, charuto, cigarrilhas, cachimbo, narguilé e outros produtores de fumaça, por indivíduos não fumantes, que convivem com fumantes em ambientes fechados, respirando as mesmas substâncias tóxicas que o fumante inala.
A fumaça do cigarro é uma mistura de aproximadamente 4.720 substâncias tóxicas diferentes que se constituem de duas fases fundamentais: a particulada e a gasosa. A fase gasosa é composta, entre outros, por monóxido de carbono, amônia, cetonas, formaldeído, acetaldeído, acroleína. A fase particulada contém nicotina e alcatrão. A nicotina é considerada pela OMS uma droga psicoativa que causa dependência. A nicotina age no sistema nervoso central, como a cocaína, com uma diferença: chega em torno de 7 a 19 segundos ao cérebro. Por isso, o tabagismo é classificado como doença e está inserido no Código Internacional de Doenças (CID-10) no grupo de transtornos mentais e de comportamento devido ao uso de substância psicoativa. Em 2011, houve um grande avanço que tem contribuído para que não haja mais a poluição tabagística ambiental nos recintos fechados. Houve a aprovação da Lei nº 12.546, de 14 de dezembro, que proíbe o fumo em local fechado em todo País. (TABAGISMO, 2019).
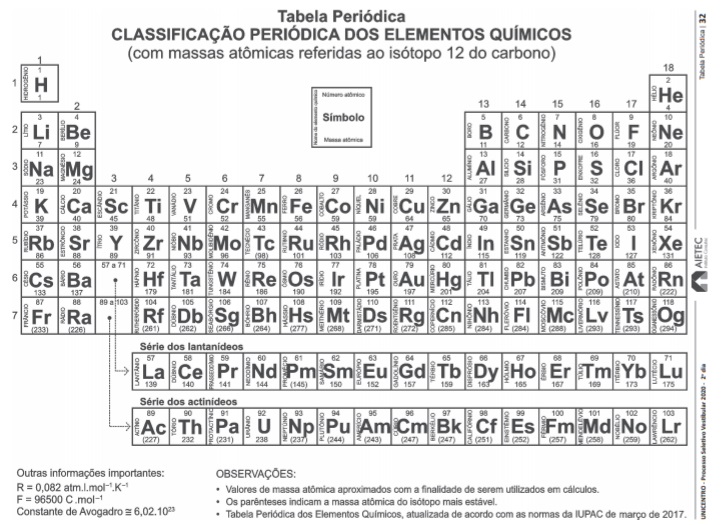
Capsaicinoides são alcaloides encontrados em vegetais e atuam conferindo picância (ardência) como mecanismo de defesa. Podem ser usados como agentes terapêuticos com ação anestésica, analgésica, psicoestimulantes e neurodepressores. Pimentas são fontes naturais de capsaicina. Sobre a capsaicina é correto afirmar:
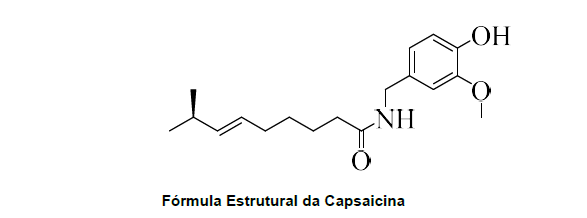
O aspartame é uma substância sintética usada como adoçante. Possui isômeros com sabor doce ou amargo. Seu isômero de sabor doce é amplamente usado em todo mundo. A molécula de aspartame é apresentada abaixo. Sobre essa molécula é correto afirmar:
Tomar um copo de suco de uva por dia pode trazer mais benefícios para saúde do que você imagina. Isso porque a fruta contém bioflavonóides, taninos e o resveratrol, substâncias que agem como proteção no organismo, reduzindo os riscos de doenças como colesterol, infartos e câncer, além de contribuir com a redução de tumores no pulmão, intestino e cólon.
A bebida também age como antioxidante, favorecendo as funções hepáticas do fígado, além de ser um valioso estimulante digestivo. O suco de uva é um forte aliado para quem se preocupa com a saúde. Confira os benefícios do suco: acelera o metabolismo, fortalece o sistema imunológico e retarda o envelhecimento.
Uma das formas de se conservar o suco de uva é através da adição do ácido sulfuroso. A reação de decomposição do ácido sulfuroso em meio aquoso, presente no suco de uva, à temperatura e pressão ambientes:
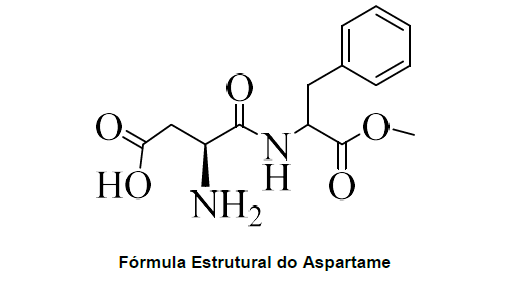
Sempre que uma substância muda de fase de agregação, a temperatura permanece constante enquanto a mudança se processa, desde que a pressão também seja mantida constante. Misturas de substâncias possuem comportamento diferente em relação às mudanças de fases. Gráficos podem ser utilizados para demonstrar essas mudanças de fases tanto de substâncias como de misturas. Observe os gráficos abaixo e marque a opção correta:
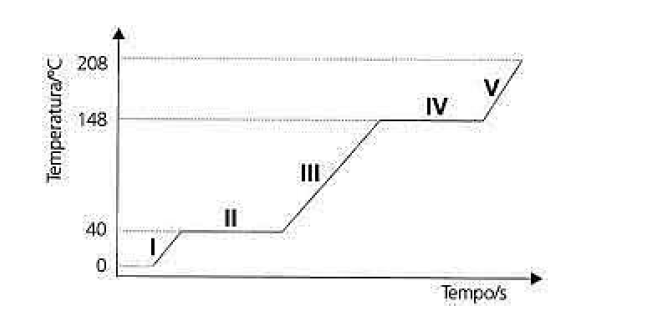 Gráfico 1 – Mudança de fases de agregação. O número I no gráfico representa o estado sólido.
Gráfico 1 – Mudança de fases de agregação. O número I no gráfico representa o estado sólido.
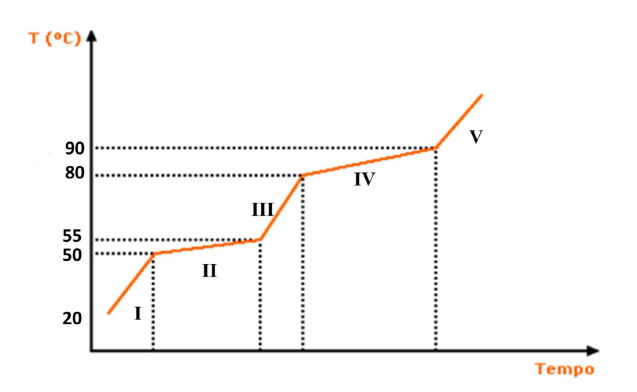
Gráfico 2 – Mudança de fases de agregação. O número I no gráfico representa o estado sólido
Muitos produtos químicos são comumente usados em nosso dia-dia por várias situações, algumas são mitos e outras são verdades:
O ácidoclorídrico (Composto X) vem da dissolução do gás cloreto de hidrogênio em água. Ele é usado em laboratório, em indústrias, na forma impura em produtos de limpeza de pisos com o nome de ácido muriático e é um dos componentes do suco gástrico do estômago.
O bicarbonato de sódio (Composto Y) é usado como antiácido, para tratar a acidez do estômago porque ele tem o poder de neutralizar os excessos do ácido clorídrico do suco gástrico, devido ao fato de ser uma substância ligeiramente alcalina(ph=9). Em algumas formulações farmacêuticas, é misturado aos ácidos cítrico e tartárico, ambos sólidos.Além do uso farmacêutico e culinário, o bicarbonato de sódio também é um ótimo auxiliar na limpeza de ambientes e de roupas. O produto tem ação anti-mancha, anti-mofo e elimina o mau cheiro.
O composto químico Hipoclorito de sódio, (Composto Z) é usado como desinfetante e como agente alvejante. Recebe o nome popular de água sanitária e é produzido pela reação de cloro com hidróxido de sódio
O vinagre (que contém ácido acético) (Composto W) pode ser usado para limpar rabiscos nas paredes, marcas de sapatos ou de móveis. O vinagre branco é uma solução rápida para remover essas manchas sobre a pintura. É preciso fazer uma mistura com a mesma quantidade de vinagre e água morna, um litro de água para quatro colheres de vinagre.
As fórmulas químicas dos compostos X, Y, Z, W são respectivamente:
O ácido oxálico (H2C2O4) está presente em caules e folhas de vegetais como o espinafre e a beterraba. Uma maneira de quantificar a concentração de ácido oxálico nos vegetais é através da titulação com hidróxido de sódio (NaOH). Para realizar uma titulação, pretende-se escolher um indicador adequado para o ponto de equivalência mostrado no gráfico. O quadro apresenta os indicadores disponíveis no laboratório.

Analise as afirmativas a seguir em relação aos números quânticos:
I. o número quântico principal corresponde aos níveis de energia do elétron e também é chamado por uma letra de acordo com o nível (K, L, M...).
II. os elementos representativos na tabela periódica possuem sua distribuição eletrônica terminando nos subníveis s e p, enquanto os elementos de transição interna terminam sua distribuição eletrônica no subnível d e os elementos de transição completam sua distribuição eletrônica no subnível f .
III. o número quântico de spin descreve o momento magnético do elétron.
IV. o número quântico magnético descreve o orbital e é a causa do ferromagnetismo das substâncias.
V. os quatro números quânticos somente assumem valores inteiros.
Assinale a alternativa CORRETA.
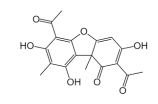
Sobre o ácido úsnico é INCORRETO afirmar que:
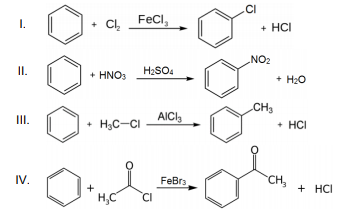
A partir da análise das reações apresentadas, assinale a alternativa CORRETA.
Em supermercados, é comum encontrar alimentos chamados de liofilizados, como frutas, legumes e carnes. Alimentos liofilizados continuam próprios para consumo após muito tempo, mesmo sem refrigeração. O termo “liofilizado”, nesses alimentos, refere‐se ao processo de congelamento e posterior desidratação por sublimação da água. Para que a sublimação da água ocorra, é necessária uma combinação de condições, como mostra o gráfico de pressão por temperatura, em que as linhas representam transições de fases.
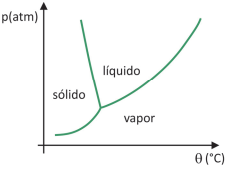
Apesar de ser um processo que requer, industrialmente, uso
de certa tecnologia, existem evidências de que os povos pré‐colombianos que viviam nas regiões mais altas dos Andes
conseguiam liofilizar alimentos, possibilitando estocá‐los por
mais tempo. Assinale a alternativa que explica como ocorria o
processo de liofilização natural:
Numa determinada condição experimental e com o catalisador adequado, ocorre uma reação, conforme representada no gráfico, que relaciona porcentagem do composto pelo tempo de reação.
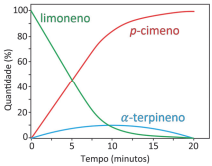
Uma representação adequada para esse processo é:

Disponível em https://www.boredpanda.com/.
Em Xangai, uma loja especializada em café oferece uma opção diferente para adoçar a bebida. A chamada sweet little rain consiste em uma xícara de café sobre a qual é pendurado um algodão‐doce, material rico em sacarose, o que passa a impressão de existir uma nuvem pairando sobre o café, conforme ilustrado na imagem.
O café quente é então adicionado na xícara e, passado um tempo, gotículas começam a pingar sobre a bebida, simulando uma chuva doce e reconfortante. A adição de café quente inicia o processo descrito, pois
Note e adote:
Temperatura de fusão da sacarose à pressão ambiente = 186 °C;
Solubilidade da sacarose a 20 °C = 1,97 kg/L de água.
CS2 + H2S + Cu → Cu2S + CH4
Com base nessa informação, julgue o próximo item
Para que a reação apresentada seja balanceada, os coeficientes estequiométricos de seus componentes devem ser iguais a 1, 2, 8, 4 e 1, da esquerda para a direita.
Com relação a princípios da química, julgue o próximo item.
Situação hipotética: Durante um experimento, um refrigerante, a uma temperatura T1, foi colocado em um copo; em seguida, outro refrigerante (de marca mesma), a uma temperatura T2, foi colocado em outro copo. Formaram-se bolhas em ambos os refrigerantes assim que estes foram despejados nos copos, mas a quantidade de bolhas formadas no refrigerante sob a temperatura T1 foi menor que a quantidade de bolhas formadas no refrigerante sob a temperatura T2. Assertiva: Nessa situação, depreende-se que T1 é maior que T2.