Questões de Vestibular Comentadas sobre química
Foram encontradas 1.427 questões
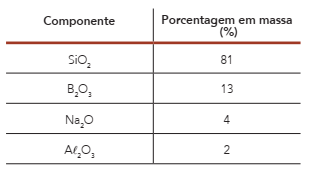
Um canudo de plástico e outro de vidro borossilicato possuem mesmo volume e densidades de 0,90 g/cm3 e 2,25 g/cm3 , respectivamente.
A razão entre as massas do canudo de plástico e do canudo de vidro corresponde a:
A tabela abaixo apresenta a composição química de uma amostra de 500 g de vidro borossilicato.
Considere as informações a seguir sobre a perfluorodecalina, substância utilizada no preparo de sangue artificial.
Fórmula mínima: C5 F9 .
Massa molar: 462 g/mol.
Sua fórmula molecular é representada por:
A lactose é hidrolisada no leite “sem lactose”, formando dois carboidratos, conforme a equação química:
lactose + água → glicose + galactose
Se apenas os carboidratos forem considerados, o valor calórico de 1 litro tanto do leite integral quanto do leite “sem lactose” é igual a −90 kcal, que corresponde à entalpia-padrão de combustão de 1 mol de lactose.
Assumindo que as entalpias-padrão de combustão da glicose e da galactose são iguais, a entalpia de combustão da glicose, em kcal/mol, é igual a:
Em seu ciclo, um átomo de carbono pode ser incorporado a diferentes compostos por meio de processos contínuos de decomposição e formação de novas moléculas. Os átomos de carbono deste caderno de prova, por exemplo, serão degradados ao longo do tempo e, posteriormente, incorporados a outros seres vivos.
Considere que, ao se degradarem, os átomos de carbono deste caderno se distribuam igualmente entre os 7,5 bilhões de habitantes do planeta.
Sabendo que o caderno possui 90 g de massa, com 45% de carbono em sua composição, o número de átomos que será incorporado em cada habitante é igual a:
Disponível em: <https://www.dicasnutricao.com.br/estimulantes-do-cha/.> Acesso em 25/03/2018.
As substâncias citadas possuem as seguintes fórmulas moleculares
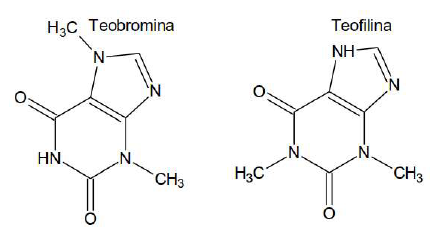
Disponível em: <http://4.bp.blogspot.com/Captura_de_tela-13.png.> Acesso em 25/03/2018.
Essas substâncias são
Na situação de equilíbrio para a reação
2S02(g) + O2(g) ⇄ 2SO3(g)
as concentrações de reagentes e produtos a 1000 K foram determinadas como sendo [SO2] = 0.27 m ol.L-1, [O2] = 0.40 mol.L-1 e [SO3] = 0.33 m ol.L-1.
Na temperatura dada, o valor da constante de equilíbrio da
reação em termos de concentração será:
A calcinação de 2.8400 g de uma mistura sólida constituída de CaCO3 e MgCO3 produziu um gás e um resíduo sólido de peso 1.5200 g.
Com essas informações, é correto afirmar que
Dois elementos genéricos X e Y apresentam as seguintes distribuições eletrônicas por camadas: X(2, 8, 8, 1) e Y(2, 8, 18, 6). Considerando-se uma provável ligação química entre esses elementos (X e Y), afirma-se:
I O átomo X ganha 1 elétron e transforma-se em um cátion monovalente.
II A fórmula do composto formado é X2Y.
III A ligação que ocorre entre eles é do tipo iônica.
IV O átomo Y cede 2 elétrons e transforma-se em um ânion bivalente.
São corretas apenas as afirmações:
Para a remoção de um esmalte, um laboratório precisa preparar 200 mL de uma solução aquosa de propanona na concentração de 0,2 mol/L. Admita que a densidade da propanona pura é igual a 0,8 kg/L.
Nesse caso, o volume de propanona pura, em mililitros, necessário ao preparo da solução corresponde a:
No tratamento dos sintomas da acidez estomacal, emprega-se o hidróxido de alumínio, que neutraliza o excesso do ácido clorídrico produzido no estômago.
Na neutralização total, a quantidade de mols de ácido clorídrico que reage com um mol de hidróxido de alumínio para formação do sal neutro corresponde a:
Recentemente, cientistas conseguiram produzir hidrogênio metálico, comprimindo hidrogênio molecular sob elevada pressão. As propriedades metálicas desse elemento são as mesmas dos demais elementos do grupo 1 da tabela de classificação periódica.
Essa semelhança está relacionada com o subnível mais energético desses elementos, que corresponde a:
Novas tecnologias de embalagens visam a aumentar o prazo de validade dos alimentos, reduzindo sua deterioração e mantendo a qualidade do produto comercializado. Essas embalagens podem ser classificadas em Embalagens de Atmosfera Modificada Tradicionais (MAP) e Embalagens de Atmosfera Modificada em Equilíbrio (EMAP). As MAP são embalagens fechadas que podem utilizar em seu interior tanto gases como He, Ne, Ar e Kr, quanto composições de CO2 e O2 em proporções adequadas. As EMAP também podem utilizar uma atmosfera modificada formada por CO2 e O2 e apresentam microperfurações na sua superfície, conforme ilustrado abaixo.

Adaptado de exclusive.multibriefs.com
Admita que, imediatamente após a colocação do gás argônio em uma embalagem específica, esse gás assume o comportamento de um gás ideal e apresenta as seguintes características:
Pressão = 1 atm
Temperatura = 300 K
Massa = 0,16 g
Nessas condições, o volume, em mililitros, ocupado pelo gás na embalagem é:

