Questões de Vestibular de Química
Foram encontradas 1.430 questões
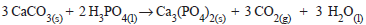
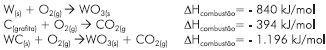
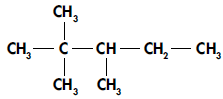
O composto orgânico, de fórmula plana abaixo, possui

Partindo da equação química ajustada e estabelecendo um consumo de 1,5 mols de pentano em 30 minutos de reação, pode-se concluir que a velocidade da reação, em mols de gás carbônico por minuto, é

De acordo com os estudos de Germain Henry Hess, professor da Universidade de São Petersburgo, no século XIX, a variação de entalpia em uma reação química depende apenas dos estados inicial e final de reagentes e de produtos da reação. A Lei de Hess contribuiu para o nascimento do princípio da conservação de energia.
A partir da aplicação da Lei de Hess, ao sistema de equações
termoquímicas I e II, é possível calcular a variação de entalpia
da reação representada pela equação química III.
Dessa forma, é correto afirmar: