Questões de Vestibular
Comentadas sobre sistemas homogêneos: solubilidade dos sais, hidrólise dos sais e curvas de titulação. em química
Foram encontradas 16 questões
DADOS QUE PODEM SER USADOS NESTA PROVA


Com base no texto e nas equações químicas, assinale a alternativa que apresenta, corretamente, o resultado experimental que comprova que a estatueta encontrada na lixeira é de bronze.
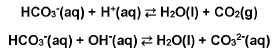
Ao adicionar carbonato de sódio na água de uma piscina, que está em condições consideradas adequadas para o banho, ocorrerá:
Em uma aula de laboratório de química, foi realizado um experimento que consistiu em adicionar em um béquer 300 g de água, em temperatura ambiente, e certa quantidade do sal sulfato de magnésio hexaidratado (MgSO4 . 6H2O) até formar uma solução saturada com corpo de fundo. Essa mistura foi aquecida até completa solubilização do sal, que ocorreu quando a temperatura atingiu 50 ºC. Na sequência, deixou-se a solução resfriar até 20 ºC e verificou-se novamente a presença do sal cristalizado no fundo do béquer.
Foram fornecidos aos alunos os dados de solubilidade desse sal nas duas temperaturas medidas.
Com as informações fornecidas, foram calculadas as massas do sal presente na solução a 50 ºC e do sal cristalizado
a 20 ºC. Esses resultados são corretamente apresentados,
nessa ordem, em:
O quadro fornece indicações sobre a solubilidade de alguns compostos iônicos inorgânicos em água a 20 ºC.
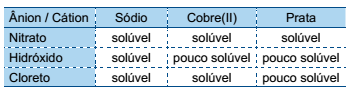
Em um laboratório, uma solução aquosa obtida a partir da
reação de uma liga metálica com ácido nítrico contém nitrato
de cobre(II) e nitrato de prata. Dessa solução, pretende-se
remover, por precipitação, íons de prata e íons de cobre(II),
separadamente. Para tanto, pode-se adicionar à mistura uma
solução aquosa de
Sob temperatura constante, acrescentou-se cloreto de sódio em água até sobrar sal sem se dissolver, como corpo de fundo. Estabeleceu-se assim o seguinte equilíbrio:
NaCℓ (s) ⇌ Na+ (aq) + Cℓ – (aq)
Mantendo a temperatura constante, foi acrescentada mais uma porção de NaCℓ (s). Com isso, observa-se que a condutibilidade elétrica da solução sobrenadante ________ , a quantidade de corpo de fundo _______________ e a concentração de íons em solução ________ .
As lacunas do texto devem ser preenchidas, respectivamente, por:
A mandioca, uma das principais fontes de carboidratos da alimentação brasileira, possui algumas variedades conhecidas popularmente como “mandioca brava”, devido a sua toxicidade. Essa toxicidade se deve à grande quantidade de cianeto de hidrogênio (HCN) liberado quando o tecido vegetal é rompido.
Após cada etapa do processamento para a produção de farinha de mandioca seca, representado pelo esquema a seguir, quantificouse o total de HCN nas amostras, conforme mostrado no gráfico que acompanha o esquema.
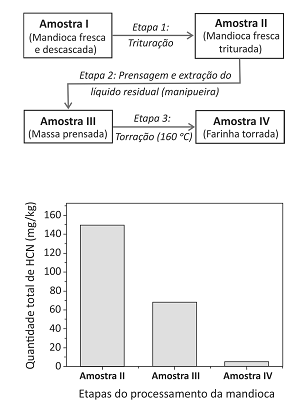
O que ocorre com o HCN nas Etapas 2 e 3?
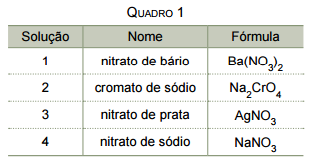
O quadro 2 apresenta o resultado das misturas, de volumes iguais, de cada duas dessas soluções.
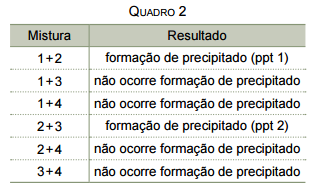
De acordo com essas informações, os precipitados formados, ppt 1 e ppt 2, são, respectivamente,
A titulação de 50 mL de uma solução aquosa de ácido clorídrico, com uma solução aquosa de hidróxido de sódio de concentração molar igual a 0,1 mol/L, utilizando fenolftaleína como indicador, está representada no gráfico a seguir.
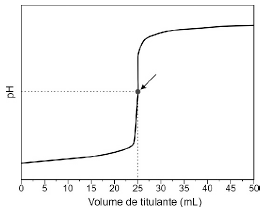
Considerando as informações do enunciado e do gráfico, assinale a alternativa correta.

Na tabela a seguir, são apresentadas informações contidas na bula de comprimidos sólidos de ibuprofeno.
cada comprimido contém
ibuprofeno____|___ 300 mg
excipientes ___|___ ácido cítrico, benzoato de sódio,dióxido de titânio e amido
Assinale a opção que apresenta o gráfico que melhor representa a variação da temperatura em função do tempo para um comprimido que tenha a composição mostrada na tabela e tenha sido macerado e aquecido.
Um técnico de laboratório distraído preparou solições de carbonato de potássio (K2CO3),
hidróxido de sódio (NaOH) e de hidróxido de cálcio (Ca(OH)2), colocando- se em três frascos não rotulados ( frascos X, Y E Z ).
Para identificar as soluções, um aluno misturou, em três tubos de ensaio distintos,
amostras de cada frasco com solução aquosa de ácido clorídrico. Nada foi observado nas soluções dos frascos X e Z, mas ocorreu uma efervenscência no
tuboque continha a solução do frasco Y.
Em seguida, o aluno combinou, dois a dois, os conteúdos de cada frasco ( frasco X, Y e Z ) em tubos de ensaios limpos.
Observou que só houve formação de precipitado quando misturou as soluções dos frascos X e Y.
Assinale a alternativa que identifica corretamente o conteúdo dos frascos X, Y e Z.
O chumbo pode ser encontrado em uma grande quantidade de tintas em forma de sais e óxidos, dentre os quais o cromato de chumbo (amarelo) e o tetróxido de trichumbo (vermelho). Uma reação de identificação do íon Pb(II) é sua precipitação em meio aquoso, que consiste na conversão de um composto de chumbo relativamente solúvel em um composto praticamente insolúvel.
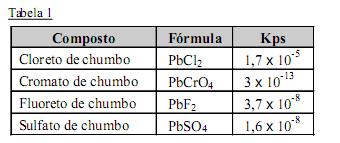
Com base nas informações acima escolha a alternativa que contém a substância mais indicada para a identificação do chumbo II por precipitação em meio aquoso. Considere que todos os sais de metais alcalinos são muito solúveis em água.
