Questões de Vestibular
Sobre transformações: estados físicos e fenômenos em química
Foram encontradas 146 questões
Sobre esse processo, é correto afirmar:
Leia o trecho do soneto “Como eu te amo”, de Gonçalves Dias, para responder a questão.
<https://tinyurl.com/y6uoquu5> Acesso em: 17.03.2018. Adaptado.
A condensação, passagem de uma substância do estado gasoso para o estado líquido, pode ocorrer quando vapores de um material entram em contato com uma superfície fria.
O verso que cita um fenômeno resultante da condensação
do vapor de água é o
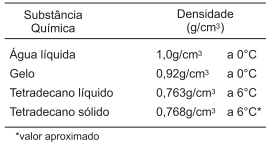
Dois tubos de ensaio fechados, sem rótulos, um contendo uma amostra de 10,0mL de água liquida, a 25oC, e outro, uma amostra de 15,0mL de tetradecano líquido, à mesma temperatura, foram colocados em um banho de gelo, após marcados aleatoriamente com os códigos XO e XB. Decorrido algum tempo, observou-se, no fundo do tubo de ensaio XB, a presença de uma fase sólida e, no tubo XO, a formação de uma fase sólida na superfície do líquido.
A partir da análise desses resultados experimentais obtidos nesses testes, é correto afirmar:
Acerca dessas informações, assinale a alternativa incorreta.
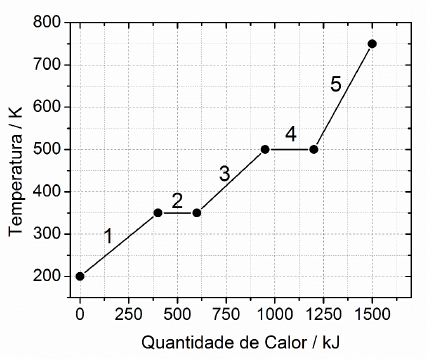
Analise as proposições em relação aos números, indicados no gráfico, referentes aos estados físicos da matéria e às suas características.
I. No estado líquido a substância assume a forma do recipiente que o contém. No gráfico, esse estado está representado pelo número 3. II. O número 2 representa mudança de estado físico, conhecida como sublimação. III. Uma das características do estado gasoso é que as partículas que formam a matéria estão bastante afastadas, dispersas no espaço. Devido a isso, nesse estado físico a matéria pode ter a forma e o volume variáveis. No gráfico, este estado físico está representado pelo número 5. IV. O número 1 representa o estado sólido, que é caracterizado por a substância apresentar volume e forma fixos. Para a amostra em questão, o estado sólido é predominante até a temperatura de 350 K. V. A ebulição está representada pelo número 4, e este processo é caracterizado pela passagem do estado líquido para o sólido.
Assinale a alternativa correta.
Na natureza, quando nos referimos às trocas de calor que ocorrem entre os corpos, existem dois tipos de transformações, as endotérmicas e as exotérmicas. Os processos que liberam calor são denominados exotérmicos e os que absorvem calor são denominados endotérmicos.
Considere as transformações físicas abaixo:
I) A evaporação da água nas salinas.
II) A sublimação da naftalina.
III) O derretimento das geleiras nos polos.
IV) A formação do orvalho.
V) O congelamento de um lago em um dia muito frio.
Quantas das alternativas anteriores correspondem a fenômenos endotérmicos?
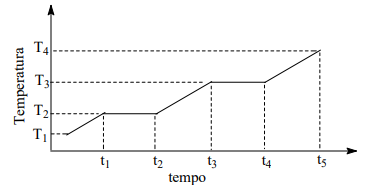
Sobre esse material e suas transformações físicas, é CORRETO afirmar:

O princípio de funcionamento dessa espécie de ar-condicionado baseia-se no fato de o gelo sofrer uma
( ) CaCO3(aq) ( ) NaOH(aq) diluído na presença de fenolftaleína ( ) limalha fina de Zn(s)
1 – mudança de cor 2 – formação de gás 3 – desaparecimento do material sólido 4 – formação de precipitado
Associando a coluna da direita com a da esquerda, a sequência correta de números é
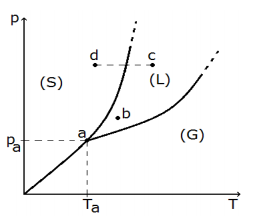
As regiões de existência de cada fase estão identificadas por (S), (L) e (G), e os pontos a, b, c e d indicam quatro estados distintos de (p,T). Considere as seguintes afirmações.
I - A substância não pode sublimar, se submetida a pressões constantes maiores do que pa.
II - A substância, se estiver no estado b, pode ser vaporizada por transformações isotérmicas ou isobáricas.
III- A mudança de estado c
 d é isobárica e
conhecida como solidificação.
Quais estão corretas?
d é isobárica e
conhecida como solidificação.
Quais estão corretas? A chuva ácida intensifica a degradação de monumentos históricos. A maioria desses monumentos é feita de mármore, que é o carbonato de cálcio na forma cristalina, CaCO3(s), e de pedra-sabão, que tem o carbonato de sódio, Na2CO3(s), como um de seus constituintes. Esses sais, CaCO3(s) e Na2CO3(s), são pouco solúveis em água, mas, em meio ácido, o íon carbonato é convertido em H2CO3, o qual, por sua vez, decompõe-se em água e CO2, conforme a equação de equilíbrio apresentada abaixo.

A partir dessas informações, e considerando que uma solução saturada de CaCO3 apresente comportamento ideal e que a constante de solubilidade do CaCO3 seja igual a 8,1 × 10-9 , julgue o item que se segue.
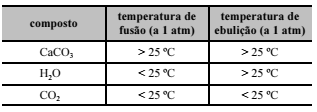
Considerando os dados apresentados na tabela abaixo, verifica-se que, a 25 ºC e 1 atm, os estados físicos do CaCO3, da H2O e do CO2 são, respectivamente, sólido, líquido e gasoso.
Nas prateleiras de supermercados é comum encontrarmos alimentos desidratados, isto é, isentos de água em sua composição. Para desidratar alimentos, é utilizado o processo de liofilização que consiste em se congelar o alimento à temperatura de -197°C e depois submeter o alimento congelado a pressões muito baixas. Na temperatura de -197°C, a água do alimento encontrase na fase sólida e, com o abaixamento de pressão, passa diretamente para a fase de vapor, sendo então eliminada.
Assinale a afirmação CORRETA:
Uma postagem de humor na internet trazia como título “Provas de que gatos são líquidos” e usava, como essas provas, fotos reais de gatos, como as reproduzidas aqui.

O efeito de humor causado na associação do título com asfotos baseia‐se no fato de que líquido
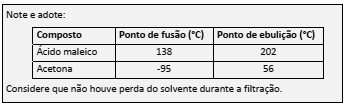
Note e adote:
Considere temperatura e pressão ambientes.
Em um experimento, determinadas massas de ácido maleico e acetona foram misturadas a 0 °C, preparando‐se duas misturas idênticas. Uma delas (X) foi resfriada a ‐78 °C, enquanto a outra (M) foi mantida a 0 °C. A seguir, ambas as misturas (M e X) foram filtradas, resultando nas misturas N e Y. Finalmente, um dos componentes de cada mistura foi totalmente retirado por destilação. Os recipientes (marcados pelas letras O e Z) representam o que restou de cada mistura após a destilação. Nas figuras, as moléculas de cada componente estão representadas por retângulos ou triângulos.
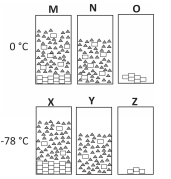
Tanto no recipiente M como no recipiente X, estão representadas soluções ___I___ de ___II___, cuja solubilidade ___III___ com a diminuição da temperatura. A uma determinada temperatura, as concentrações em M e N e em X e Y são ___IV___. Em diferentes instantes, as moléculas representadas por um retângulo pertencem a um composto que pode estar ___V___ ou no estado ___VI___.
As lacunas que correspondem aos números de I a VI devem ser corretamente preenchidas por: