Questões de Vestibular UNC 2011 para Vestibular, Verão
Foram encontradas 7 questões
No jornal O Estado de São Paulo, de 30 de agosto de 2011, foi publicada uma reportagem sobre o acidente nuclear na usina Daiichi, em Fukushima no Japão “[...] em 33 localidades havia um excesso de césio-137 de 1,48 milhão de becquerel por metro quadrado, [...]”.
Com base no texto acima e nos conceitos sobre processos radioativos, analise as afirmações a seguir.
I - O césio-137 é um material radioativo com tempo de meia vida curto e não apresenta risco à saúde das pessoas que moram na região afetada pelo acidente.
II- A partícula α possui estrutura semelhante ao núcleo do átomo de hélio.
III- Processos radioativos são essencialmente transformações nucleares, na qual núcleos instáveis emitem radiações.
IV- Bequerel é uma grandeza que mede a intensidade de radiação ou a atividade radioativa.
Assinale a alternativa correta.
No jornal O Estado de São Paulo, de 16 de junho de 2011, foi publicada uma reportagem sobre uma apreensão de drogas sintéticas “[...] A Polícia Federal (PF) apreendeu cerca de 9,2 quilos de metanfetamina e 26.985 pontos de LSD, na última terça-feira, no Aeroporto Internacional de São Paulo, em Guarulhos - SP. Essa foi a primeira apreensão de drogas sintéticas este ano na rota de entrada no Brasil por esse aeroporto. [...]”.
Com base nos conceitos químicos e no texto acima, analise as afirmações a seguir.
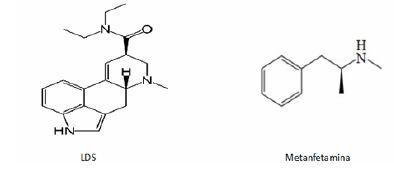
I- Tanto a metanfetamina quanto o LSD apresentam a função química amida.
II- A metanfetamina e o LSD não apresentam o fenômeno da ressonância.
III- C20H25N3O é a fórmula molecular do LSD.
IV- A metanfetamina possui fórmula molecular C10H15N.
Assinale a alternativa correta.
O texto abaixo está presente na legislação que institui o Código de Trânsito Brasileiro- CTB.
“[...]Conduzir veículo automotor, na via pública, estando com concentração de álcool por litro de sangue igual ou superior a 6 (seis) decigramas, ou sob a influência de qualquer outra substância psicoativa que determine dependência: Penas - detenção, de seis meses a três anos, multa e suspensão ou proibição de se obter a permissão ou a habilitação para dirigir veículo automotor. [...]”
Um condutor automotivo parado em uma operação policial, após ser submetido a análises técnicas, apresentou uma concentração de 21 decigramas de álcool por litro de sangue.
Com base no texto acima e nos conceitos químicos, analise as afirmações a seguir.
I- A concentração de álcool no sangue desse condutor é de 2,1μg/μL.
II- O condutor deverá ser penalizado segundo a legislação do CTB.
III- Caso o condutor possua em seu organismo um volume de sangue igual a 5,0 L, a quantidade de álcool presente em seu corpo é de 10,5 g.
IV - A combustão completa do etanol geral CO e água.
Assinale a alternativa correta.
Baseado no texto e nas reações acima, juntamente com os conceitos químicos, analise as afirmações a seguir.
I- No cátodo o etanol é oxidado a etanal.
II- No ânodo ocorre uma reação de redução.
III- O sentido da corrente elétrica (i) é do ânodo para o cátodo.
IV- Na reação global corresponde a uma reação de combustão incompleta do etanol.
Assinale a alternativa correta.
Quantos elétrons são produzidos a partir da oxidação de 460 μg de etanol no interior de um bafômetro informado no texto acima.?
Dado: número de Avogrado: 6.1023 CH3CH2OH = 46 g/mol
No jornal Folha de São Paulo, de 16 de setembro de 2011, foi publicada uma reportagem sobre o Shopping Center Norte de São Paulo - SP “[...] Segundo a Cetesb, foi encontrado gás metano no terreno, que serviu como depósito de lixo na década de 1980, antes da construção do shopping [...]”.
Dado: CH4 = 16g/mol, Entalpia de combustão do metano = - 889,5 kJ/mol
Com base no texto acima e nos conceitos químicos, analise as afirmações a seguir.
I- O gás metano é uma molécula apolar, possui estrutura tetraédrica e fórmula molecular CH4.
II- O gás metano é um dos principais gases presentes no biogás.
III- A energia liberada na combustão de 100 Kg de metano é +5,56.106 kJ, aproximadamente.
IV- Caso a concentração do gás metano na região do shopping seja elevada, há o risco de ocorrer explosões.
Assinale a alternativa correta.
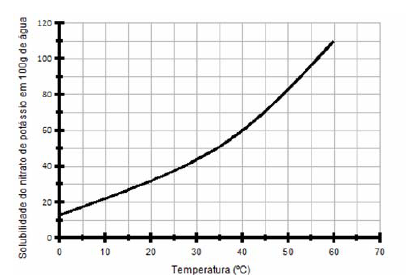
Um técnico preparou 420g de uma solução saturada de nitrato de potássio (KNO3, dissolvida em água) em um béquer a uma temperatura de 60ºC. Depois deixou a solução esfriar até uma temperatura de 40ºC, verificando a presença de um precipitado.
A massa aproximada desse precipitado é:
(desconsidere a massa de água presente no precipitado)