Questões de Vestibular CEDERJ 2017 para Vestibular - Segundo Semestre
Foram encontradas 8 questões
Um volume de 16.42 mL de uma solução de permanganato de potássio 0.1327 M é necessário para oxidar 20.00 mL de uma solução de FeSO4 em meio ácido.
Considere que a equação não balanceada representativa da reação é:
Fe2+ + MnO4 − + H+ → Mn2+ + Fe3+ + H2O
A concentração da solução do sal de ferro será
aproximadamente:
Tem-se a seguinte célula: Mn2+ (0.1 M) + O2 (1 atm) + 2H2O ⇄ MnO2 + H2O2 (0.1 M) + 2H+ (0.1 M).
Considere que na temperatura ambiente os valores dos potenciais padrão das espécies constituintes da célula, são:
O2 + 2H+ + 2e− ⇄ H2O2 E0 = + 0.68 V
MnO2 + 4H+ + 2e− ⇄ Mn2+ + 2H2O E0 = + 1.23 V
A direção que a reação vai tomar e o potencial
gerado são respectivamente:
Na produção de sabão, uma amostra de 100 g de hidróxido de sódio reage com a estearina, de acordo com a reação não balanceada a seguir:
(C17H35COO)3C3 H5(s) + NaOH(aq) → C17H35COONa(s) + C3H5 (OH)3( l )
Considerando que, a partir de 100 g de hidróxido de
sódio, foram obtidos 512 g de estearato de sódio, o rendimento
deste procedimento é aproximadamente igual a
A seguir são apresentados nomes de alguns aldeídos e cetonas que podem ser preparados por oxidação de um álcool adequado: etanol, propanona, 2-metilpropanal e 2-pentanona.
A opção que apresenta as fórmulas estruturais dos álcoois que dão origem, por oxidação, aos compostos citados na ordem apresentada é:
Alguns dos efeitos fisiológicos da testosterona podem ser aumentados pelo uso de alguns de seus derivados sintéticos: os anabolizantes. Estas substâncias provocam aumento da massa muscular e diminuição da gordura. Seu uso indiscriminado, porém, pode provocar efeitos colaterais sérios, como hipertensão, edemas, distúrbios do sono e acne. Seu uso prolongado leva a danos irreversíveis ao fígado e à diminuição na produção do esperma. Analise as estruturas abaixo.
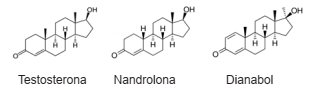
A opção que indica as funções comuns nos três
compostos é:
O sulfeto de níquel (II), NiS, ocorre na natureza como um mineral relativamente raro, a millerita. Uma de suas ocorrências é em meteoritos. Para se determinar a quantia de NiS em uma amostra do mineral, ela é tratada com ácido nítrico para liberar o níquel.
NiS(s) + 4HNO3(aq) → Ni(NO3)2(aq) + S(s) + 2NO2(g) + 2H2O(l)
A solução aquosa de Ni(NO3)2 é então tratada com o composto orgânico dimetilglioxima (C4H8N2O2 – DMG) para formar o sólido vermelho Ni(C4 H7N2O2 )2(s) de acordo com a reação:
Ni(NO3 )2(aq) + 2 C4 H8 N2 O2(aq) → Ni(C4 H7 N2 O2 ) 2(s) + 2 HNO3(aq
Se uma amostra de 0.468 g contendo millerita
produz 0.206 g do sólido vermelho Ni(C4
H7
N2
O2
)2(s) , a
porcentagem de NiS na amostra é:
O Halotano, C2HBrClF3 , é um gás não inflamável, não explosivo, e não irritante que é geralmente usado como anestésico, por inalação. Suponha que se faça a mistura de 15.0 g de vapor de Halotano com 23.5 g do gás oxigênio sendo que a pressão total da mistura seja igual a 855 mmHg.
Nas condições apresentadas as pressões parciais do halotano e do oxigênio na mistura serão, respectivamente: