Questões de Vestibular CESMAC 2016 para Prova Medicina-2016.2- 2° DIA- PROVA TIPO 1
Foram encontradas 60 questões
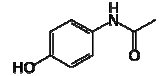
Uma rota de síntese sugerida para este composto é a reação de p-aminofenol com anidrido acético. Com base nas informações acima, podemos dizer que o paracetamol:
HCO3 – (aq) + H2O(l)
 CO3
2–(aq) + H3O
+
(aq)
CO3
2–(aq) + H3O
+
(aq) A respeito de uma solução em que as concentrações de carbonato (CO3 2–) e bicarbonato (HCO3 – ) são iguais, podemos dizer que:
CH3CH2OH + OH· → H2O + CH3CHOH·
Sobre esta reação, podemos afirmar o que segue.
Zz com número atômico 19 e
Yy com número atômico 17.
Analise cada uma das seguintes afirmativas. 1) Zz é um metal. 2) O elemento Yy está localizado no 3º período da tabela periódica. 3) O elemento Yy possui eletronegatividade menor que o elemento Zz 4) Yy é um halogênio
Estão corretas apenas
NaHCO3(s) → NaOH(s) + CO2(g)
Qual o volume em litros de gás carbônico produzido a uma temperatura de 27 °C e uma pressão de 1 atm pela decomposição de 4,2 g de bicarbonato de sódio (massa molar 84,00 g mol–1)?
1) Sólidos iônicos geralmente são formados entre um elemento com grande número de orbitais vazios, na camada de valência, e um elemento com poucos orbitais vazios, na camada de valência. 2) Elementos muito eletronegativos tendem a formar compostos moleculares entre si. 3) Sólidos cristalinos não apresentam ordem definida no posicionamento dos átomos. 4) Líquidos que realizam ligações de hidrogênio intermolecular tendem a apresentar maiores pontos de ebulição.
Estão corretas
1) Areia e sal de cozinha 2) Areia e ar 3) Água e sal de cozinha 4) Óleo de soja e água
( ) Filtração ( ) Destilação ( ) Dissolução seguida de filtração ( ) Decantação
A sequência correta é:
A remoção de metais pesados de um efluente, muitas vezes, pode ser feita pela precipitação do elemento na forma de um composto pouco solúvel. Considere o exemplo do chumbo, na forma de íon bivalente positivo, que possui vários compostos insolúveis:
Composto Produto de Solubilidade (Kps)
PbCl2 1,6x10–5
PbSO4 1,6x10–8
PbS 8,8x10–29