Questões de Vestibular UFSC 2011 para Vestibular - História / Geografia / Física / Quimica
Foram encontradas 70 questões
Durante a última parte da viagem, Eduardo pega um pacote contendo 40g de biscoito e lê o rótulo. A tabela que Eduardo vê foi adaptada e está representada a seguir:
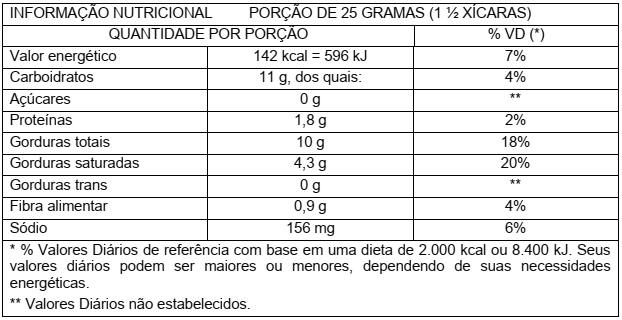
Considere que o total de gordura refere-se apenas a triglicerídeos. Com base nas informações acima, assinale a proposição CORRETA.
Segundo o rótulo do produto, seriam necessários mais de 30 pacotes de biscoito para suprir
a necessidade energética.
Durante a última parte da viagem, Eduardo pega um pacote contendo 40g de biscoito e lê o rótulo. A tabela que Eduardo vê foi adaptada e está representada a seguir:
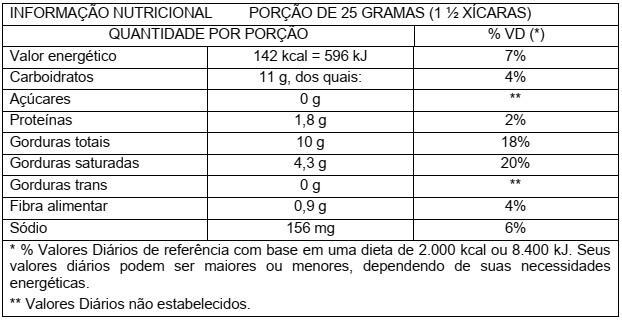
Considere que o total de gordura refere-se apenas a triglicerídeos. Com base nas informações acima, assinale a proposição CORRETA.
Considerando que todo o sódio indicado no rótulo está na forma de cloreto de sódio, pode-se
afirmar que há 140 mg de cloreto na porção indicada.
Durante a última parte da viagem, Eduardo pega um pacote contendo 40g de biscoito e lê o rótulo. A tabela que Eduardo vê foi adaptada e está representada a seguir:
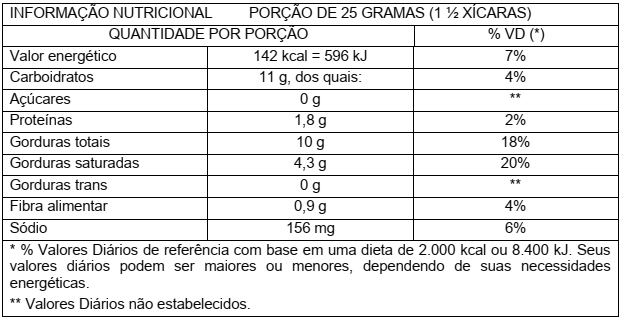
Considere que o total de gordura refere-se apenas a triglicerídeos. Com base nas informações acima, assinale a proposição CORRETA.
A porção contém 11 gramas de carboidratos e 0 grama de açúcares, o que demonstra que
açúcares não são carboidratos.
Durante a última parte da viagem, Eduardo pega um pacote contendo 40g de biscoito e lê o rótulo. A tabela que Eduardo vê foi adaptada e está representada a seguir:
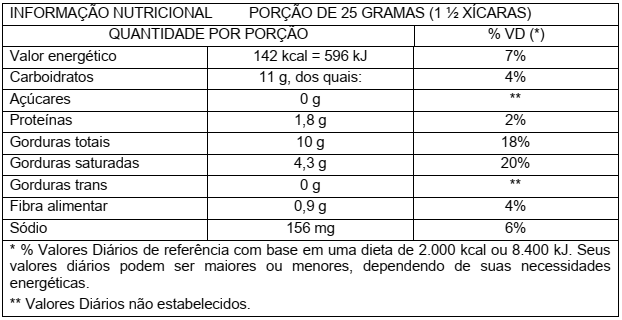
Considere que o total de gordura refere-se apenas a triglicerídeos. Com base nas informações acima, assinale a proposição CORRETA.
O rótulo apresenta um erro na massa da porção.
Chegando ao apartamento dos pais em Florianópolis, Carlos resolve fazer um café. Coloca água
para ferver e aguarda. Algum tempo depois comenta: “- Essa água parece que demora mais para
ferver aqui do que em Urubici!”.
Com base nas propriedades físicas das substâncias, é CORRETO afirmar que:
numa altitude menor a camada de ar sobre o local é maior, logo a temperatura de ebulição
da água é maior.
Chegando ao apartamento dos pais em Florianópolis, Carlos resolve fazer um café. Coloca água para ferver e aguarda. Algum tempo depois comenta: “- Essa água parece que demora mais para ferver aqui do que em Urubici!”.
Com base nas propriedades físicas das substâncias, é CORRETO afirmar que:
a pressão de vapor de um líquido não é dependente da temperatura.
Chegando ao apartamento dos pais em Florianópolis, Carlos resolve fazer um café. Coloca água para ferver e aguarda. Algum tempo depois comenta: “- Essa água parece que demora mais para ferver aqui do que em Urubici!”.
Com base nas propriedades físicas das substâncias, é CORRETO afirmar que:
devido às forças intermoleculares, o ponto de ebulição da água é maior que o do H2S.
Chegando ao apartamento dos pais em Florianópolis, Carlos resolve fazer um café. Coloca água para ferver e aguarda. Algum tempo depois comenta: “- Essa água parece que demora mais para ferver aqui do que em Urubici!”.
Com base nas propriedades físicas das substâncias, é CORRETO afirmar que:
um líquido entra em ebulição quando sua pressão de vapor é menor que a pressão
atmosférica.
Chegando ao apartamento dos pais em Florianópolis, Carlos resolve fazer um café. Coloca água para ferver e aguarda. Algum tempo depois comenta: “- Essa água parece que demora mais para ferver aqui do que em Urubici!”.
Com base nas propriedades físicas das substâncias, é CORRETO afirmar que:
uma mistura de água com açúcar tem ponto de ebulição maior que água pura.
Chegando ao apartamento dos pais em Florianópolis, Carlos resolve fazer um café. Coloca água para ferver e aguarda. Algum tempo depois comenta: “- Essa água parece que demora mais para ferver aqui do que em Urubici!”.
Com base nas propriedades físicas das substâncias, é CORRETO afirmar que:
o Mar Morto, na Jordânia, localiza-se a uma altitude de -395 metros, assim, o ponto de
ebulição da água neste local deve ser maior que 100 °C.