Questões de Vestibular FGV 2020 para Graduação em Economia - Química e Língua Portuguesa - 1º Dia
Foram encontradas 15 questões
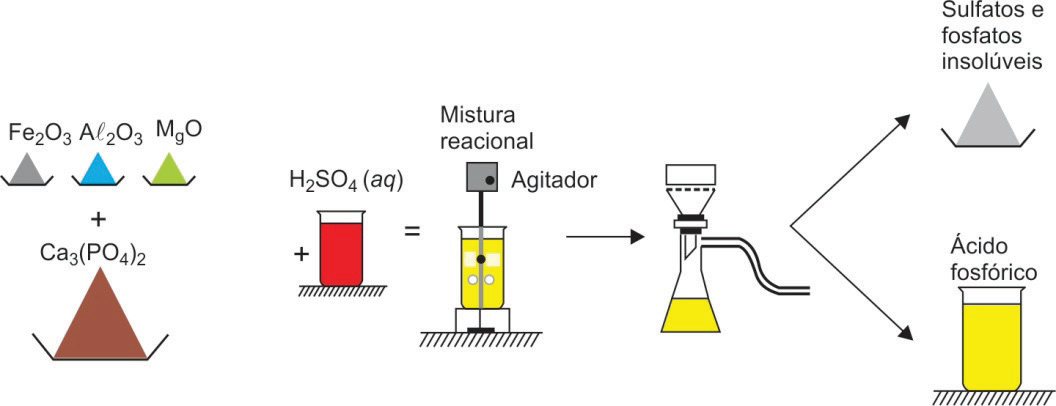
(Nilson Fernandes et al. “Effect of the impurities on the phosphoric acid process”. Materials Science Forum, 2012. Adaptado.)
A classificação do produto obtido nessa mistura reacional em relação às suas fases e o número total de elétrons do íon metálico bivalente dentre os cátions dos óxidos utilizados na formação da mistura reacional são
Dados: Fe Z = 26 Al Z = 13 Mg Z = 12
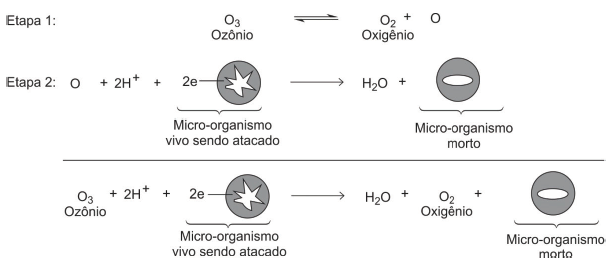
(Ervim Lenzi e Luzia Otilia B. Favero. Introdução à química da atmosfera: ciência, vida e sobrevivência, 2019. Adaptado.)
Considerando-se as informações e o esquema apresentado na figura, a molécula de ozônio apresenta
Dado: massa molar Ca = 40 g/mol
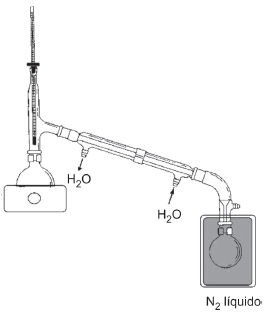
Após alcançado o equilíbrio térmico no interior do recipiente de coleta, o valor percentual da pressão em seu interior, em relação à pressão inicial, será, aproximadamente,
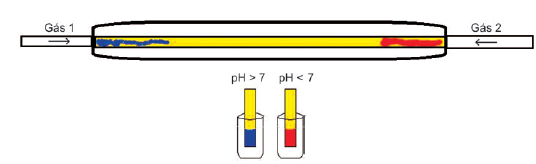
Os gases 1 e 2 empregados no experimento podem ser, respectivamente,
O produto de decaimento do samário-153 é o ________________ , e o tempo de meia-vida do iodo-131 corresponde a __________________ tempo de meia-vida do samário-153.
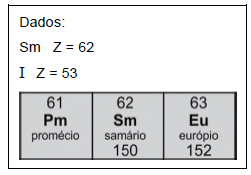
As lacunas são preenchidas por:
2ClO (g) ⇌ (ClO)2 (g)
Os dados de reações de dimerização do gás monóxido de cloro em diferentes temperaturas estão indicados na tabela.
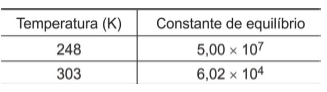
O processo de dimerização do gás monóxido de cloro é
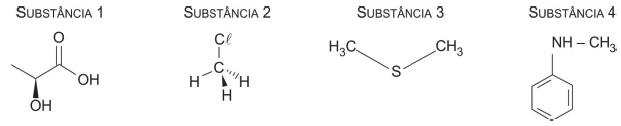
Entre essas substâncias, formarão interações intermoleculares do tipo ligação de hidrogênio com a água apenas as indicadas por
Cl2 (g) + NaOH (aq) + H2O (l) → NaClO·5H2O(s) + NaCl (s)
Na preparação de 1 mol de hipoclorito de sódio pentaidratado, a quantidade de água que reage e a quantidade de cloreto de sódio que se forma são, respectivamente,
Considerando-se que a 25 °C o produto iônico da água (Kw) é igual a 1 × 10–14, as quantidades de íons H+ e de íons OH– presentes nessa garrafa de água são, respectivamente,
O esquema apresenta uma célula a combustível de ureia, as semirreações e seus potenciaispadrão de redução.
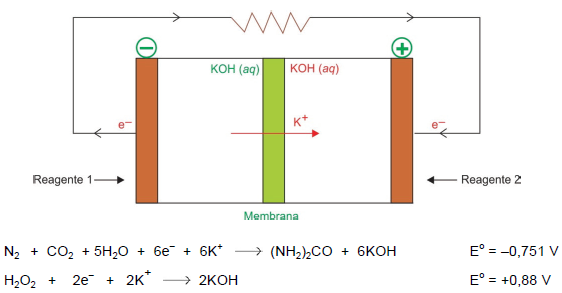
(Ke Ye et al. “Recent Advances in the electro-oxidation of urea for direct urea fuel cell and urea electrolysis”. Topics in Current Chemistry, 2018. Adaptado.)
O potencial-padrão dessa célula a combustível e todos os produtos da reação global são, respectivamente,
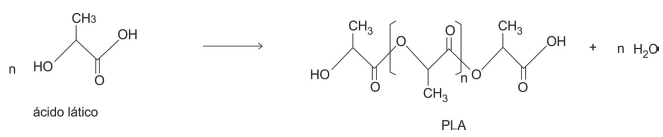
O PLA é biodegradável e demora cerca de seis meses para se decompor, enquanto a degradação dos plásticos convencionais, como o poliestireno (PS), pode demorar até mil anos. A classificação da reação de formação do PLA e a fórmula estrutural do monômero que resulta no PS são
CaO (s) + 3C (s) → CaC2 (s) + CO (g)
Em um experimento em um reator aberto, verificou-se que a diferença entre a massa da mistura reacional e a massa do conteúdo no reator ao término da reação foi 1 400 g.
Dados: massa molar C = 12 g/mol massa molar O = 16 g/mol massa molar Ca = 40 g/mol
A massa de carbono que reagiu foi igual a
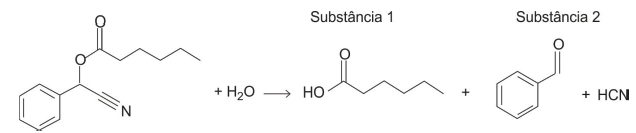
A cadeia carbônica da substância 1 é classificada como __________________ e __________________ . A oxidação da substância 2 resulta em um composto que pertence à função orgânica __________________ .
As lacunas são preenchidas, respectivamente, por