Questões de Vestibular USP 2016 para Vestibular - Primeira Fase
Foram encontradas 14 questões
A figura foi obtida em uma câmara de nuvens, equipamento
que registra trajetórias deixadas por partículas
eletricamente carregadas. Na figura, são mostradas as
trajetórias dos produtos do decaimento de um isótopo do
hélio 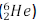 em repouso: um elétron (e-) e um isótopo de lítio
em repouso: um elétron (e-) e um isótopo de lítio
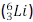 , bem como suas respectivas quantidades de
movimento linear, no instante do decaimento,
representadas, em escala, pelas setas. Uma terceira
partícula, denominada antineutrino (
, bem como suas respectivas quantidades de
movimento linear, no instante do decaimento,
representadas, em escala, pelas setas. Uma terceira
partícula, denominada antineutrino (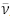 , carga zero), é
também produzida nesse processo.
, carga zero), é
também produzida nesse processo.
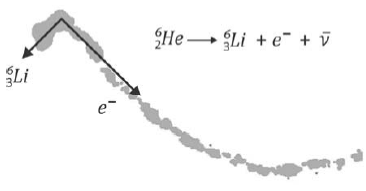
O vetor que melhor representa a direção e o sentido da
quantidade de movimento do antineutrino é
Reatores nucleares não são exclusivamente criações humanas. No período pré✄cambriano, funcionou na região de Oklo, África, durante centenas de milhares de anos, um reator nuclear natural, tendo como combustível um isótopo do urânio.
Para que tal reator nuclear natural pudesse funcionar, seria necessário que a razão entre a quantidade do isótopo físsil(235U) e a do urânio 238U fosse cerca de 3%. Esse é o enriquecimento utilizado na maioria dos reatores nucleares,refrigerados a água, desenvolvidos pelo homem.
O 235U decai mais rapidamente que o 238U; na Terra,atualmente, a fração do isótopo 235U, em relação ao 238U, é cerca de 0,7%. Com base nessas informações e nos dados fornecidos, pode-se estimar que o reator natural tenha estado em operação há
Note e adote: M(t) = M(0)10-λt ; M(t) é a massa de um isótopo radioativo no instante t. λ descreve a probabilidade de desintegração por unidade de tempo.
Para o 238U, λ238 = 0,8 x 10-10 ano-1.
Para o 235U, λ235 = 4,0 x 10-10 ano-1.
log10 (0,23) = – 0,64
No início do século XX, Pierre Curie e colaboradores, em uma
experiência para determinar características do recém-descoberto elemento químico rádio, colocaram uma
pequena quantidade desse material em um calorímetro e
verificaram que 1,30 grama de água líquida ia do ponto de
congelamento ao ponto de ebulição em uma hora. A
potência média liberada pelo rádio nesse período de tempo
foi, aproximadamente,
Note e adote:
Calor específico da água: 1 cal/(g ºC)
1 cal = 4 J
Temperatura de congelamento da água: 0 ºC
Temperatura de ebulição da água: 100 ºC
Considere que toda a energia emitida pelo rádio foi absorvida pela água
e empregada exclusivamente para elevar sua temperatura.
Na estratosfera, há um ciclo constante de criação e destruição do ozônio. A equação que representa a destruição do ozônio pela ação da luz ultravioleta solar (UV) é
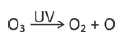
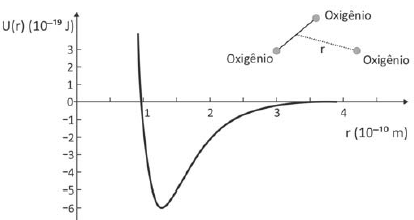
O gráfico representa a energia potencial de ligação entre um dos átomos de oxigênio que constitui a molécula de O3 e os outros dois, como função da distância de separação r.
A frequência dos fótons da luz ultravioleta que corresponde à energia de quebra de uma ligação da molécula de ozônio para formar uma molécula de O2 e um átomo de oxigênio é, aproximadamente,
Note e adote:
E = hf
E é a energia do fóton.
f é a frequência da luz.
Constante de Planck, h = 6 x 10-34 J.s
Dependendo do pH do solo, os nutrientes nele existentes podem sofrer transformações químicas que dificultam sua absorção pelas plantas. O quadro mostra algumas dessas transformações, em função do pH do solo.
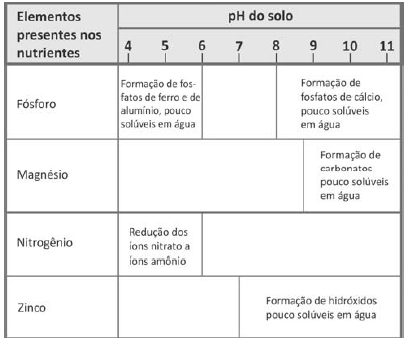
Para que o solo possa fornecer todos os elementos citados
na tabela, o seu pH deverá estar entre
Em ambientes naturais e na presença de água e gás oxigênio, a pirita, um mineral composto principalmente por dissulfeto de ferro (FeS2), sofre processos de intemperismo, o que envolve transformações químicas que acontecem ao longo do tempo.
Um desses processos pode ser descrito pelas transformações sucessivas, representadas pelas seguintes equações químicas:
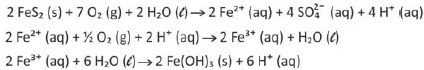
Considerando a equação química que representa a
transformação global desse processo, as lacunas da frase
“No intemperismo sofrido pela pirita, a razão entre as
quantidades de matéria do FeS2(s) e do O2(g) é __________,
e, durante o processo, o pH do solo __________” podem ser
corretamente preenchidas por
Um estudante realizou um experimento para avaliar a reatividade dos metais Pb, Zn e Fe. Para isso, mergulhou, em separado, uma pequena placa de cada um desses metais em cada uma das soluções aquosas dos nitratos de chumbo, de zinco e de ferro. Com suas observações, elaborou a seguinte tabela, em que (sim) significa formação de sólido sobre a placa e (não) significa nenhuma evidência dessa formação:

A seguir, montou três diferentes pilhas galvânicas, conforme esquematizado.

Nessas três montagens, o conteúdo do béquer I era uma solução aquosa de CuSO4 de mesma concentração, e essa solução era renovada na construção de cada pilha. O eletrodo onde ocorria a redução (ganho de elétrons) era o formado pela placa de cobre mergulhada em CuSO4 (aq). Em cada uma das três pilhas, o estudante utilizou, no béquer II, uma placa de um dos metais X (Pb, Zn ou Fe), mergulhada na solução aquosa de seu respectivo nitrato.
O estudante mediu a força eletromotriz das pilhas, obtendo os valores: 0,44 V; 0,75 V e 1,07 V.
A atribuição correta desses valores de força eletromotriz a
cada uma das pilhas, de acordo com a reatividade dos metais
testados, deve ser
Em uma aula experimental, dois grupos de alunos (G1 e G2) utilizaram dois procedimentos diferentes para estudar a velocidade da reação de carbonato de cálcio com excesso de ácido clorídrico. As condições de temperatura e pressão eram as mesmas nos dois procedimentos e, em cada um deles, os estudantes empregaram a mesma massa inicial de carbonato de cálcio e o mesmo volume de solução de ácido clorídrico de mesma concentração.
O grupo G1 acompanhou a transformação ao longo do tempo, realizada em um sistema aberto, determinando a variação de massa desse sistema (Figura 1 e Tabela).
O grupo G2 acompanhou essa reação ao longo do tempo, porém determinando o volume de dióxido de carbono recolhido (Figura 2).
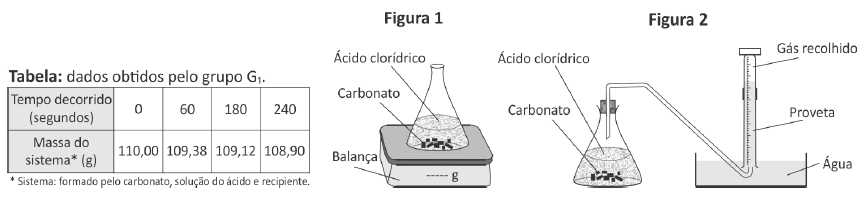
Comparando os dois experimentos, os volumes aproximados de CO2, em litros, recolhidos pelo grupo G2 após 60, 180 e 240 segundos devem ter sido, respectivamente,
Note e adote:
massa molar do CO2: 44 g/mol;
volume molar do CO2: 24 L/mol;
desconsidere a solubilidade do CO2 em água.
Note e adote: Composição aproximada do ar em volume: 80% de N2 e 20% de O2.
Para aumentar o grau de conforto do motorista e contribuir para a segurança em dias chuvosos, alguns materiais podem ser aplicados no para-brisa do veículo, formando uma película que repele a água. Nesse tratamento, ocorre uma transformação na superfície do vidro, a qual pode ser representada pela seguinte equação química não balanceada:
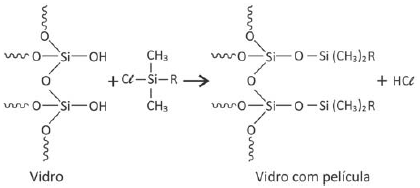
Das alternativas apresentadas, a que representa o melhor material a ser aplicado ao vidro, de forma a evitar o acúmulo de água, é:
Note e adote:
R = grupo de átomos ligado ao átomo de silício.
Sob certas condições, tanto o gás flúor quanto o gás cloro podem reagir com hidrogênio gasoso, formando,respectivamente, os haletos de hidrogênio HF e HCl, gasosos. Pode-se estimar a variação de entalpia (ΔH) de cada uma dessas reações, utilizando-se dados de energia deligação. A tabela apresenta os valores de energia de ligação dos reagentes e produtos dessas reações a 25 ºC e 1 atm.

Com base nesses dados, um estudante calculou a variação de entalpia (ΔH) de cada uma das reações e concluiu,corretamente, que, nas condições empregadas.
Células a combustível são opções viáveis para gerar energia elétrica para motores e outros dispositivos. O esquema representa uma dessas células e as transformações que nela ocorrem.
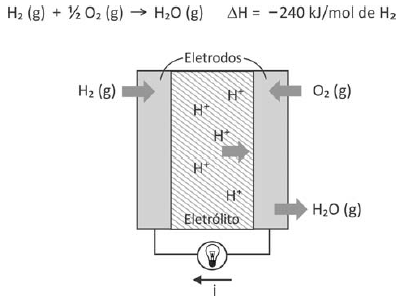
A corrente elétrica (i), em ampère (coulomb por segundo), gerada por uma célula a combustível que opera por 10 minutos e libera 4,80 kJ de energia durante esse período de tempo, é
Note e adote:
Carga de um mol de elétrons = 96.500 coulomb.
A dopamina é um neurotransmissor importante em processos cerebrais. Uma das etapas de sua produção no organismo humano é a descarboxilação enzimática da L-Dopa, como esquematizado:
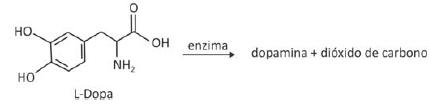
Sendo assim, a fórmula estrutural da dopamina é: