Questões de Vestibular UEFS 2010 para Vestibular, Prova 03
Foram encontradas 60 questões
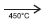 2HI(g) v = k[H2] [I2]
2HI(g) v = k[H2] [I2] O modelo da teoria das colisões, que resultou de estudos dos fatores que influem na velocidade das reações químicas, é uma explicação para o modo como as moléculas de reagentes são clivadas e são formadas as moléculas de produtos de uma reação química.
Admitindo-se a reação química elementar entre o hidrogênio e o iodo, a 450oC, representada pela equação química, a expressão da lei de velocidade dessa reação, e com base na teoria das colisões, para que essa reação ocorra, dentre outros fatores, é preciso que
Em um recipiente de 2,0L, foram misturados 12,0mol de dióxido de enxofre, SO2(g), com 10,0mol de oxigênio, O2(g), à determinada temperatura. Após ter sido fechado o recipiente, e depois de estabelecido o equilíbrio químico, o sistema, representado pela equação química, apresentou 8,0mol de trióxido de enxofre, SO3.
A partir dessas informações e da análise do equilíbrio químico do sistema considerado, é correto afirmar:
Ácido Halogenídrico Constante de ionização, Ka, a 25º C
HF (aq) 6,0.10-4
HC (aq) 1,0.107
HBr (aq) 1,0.109
HI (aq) 3,0.109
A tabela relaciona os valores da constante de ionização, Ka, dos ácidos halogenídricos.
A partir da análise dessa tabela, é correto afirmar:
COOH
Ácido Cítrico
O ácido cítrico, responsável pela acidez das frutas cítricas, é utilizado como acidificante e flavorizante no processamento de alguns alimentos.
A partir dessas informações, é correto afirmar:
O acarajé, preparado no óleo de dendê aquecido à ebulição, é um alimento rico em proteínas e carboidratos, de grande valor nutricional, que só a baiana do acarajé sabe preparar.
A partir dessa informação, é correto afirmar: