Questões de Vestibular UERJ 2014 para Vestibular, Primeiro Exame - Espanhol
Foram encontradas 60 questões
No início do texto, ao expressar sua indignação em relação ao tema abordado, o autor apresenta uma reflexão sobre o emprego de adjetivos.
Essa reflexão está associada à seguinte ideia:
É uma imagem verdadeiramente surreal, (l. 17)
Na argumentação desenvolvida pelo autor, a imagem do porta-malas do carro da polícia expressa sentidos ambivalentes em relação à violência.
Esses sentidos podem ser definidos como:
Pois assim como Amarildo é aquele que desapareceu das vistas, e não faz muito tempo, Cláudia é aquela que subitamente salta à vista, e ambos soam, queira-se ou não, como o verso e o reverso do mesmo. (l. 22-24)
Neste trecho, para aproximar dois casos recentemente noticiados na imprensa, o autor emprega um recurso de linguagem denominado:
No texto, o significado de cada termo se caracteriza por ser, respectivamente:
Nessa associação, a imagem do poste se constrói pelo seguinte recurso da linguagem:
No entanto, no decorrer do poema, a visão predomina sobre a audição.
Os dois elementos que confirmam isso são:
Agora ele estava tão verdinho! (v. 4)
De modo diferente do que ocorre em passarinhos, o emprego do diminutivo, no verso acima, contribui para expressar um sentido de:
La idea de que se hace una re-reforma se verifica en el siguiente fragmento:
“Miles salen a las calles contra todo”. (l. 32)
El titular de la noticia resume la insatisfacción de los brasileños respecto a la situación actual del país.
La palabra que se acerca al sentido de ese sentimiento de insatisfacción es:
En la cohesión textual, se llama anáfora al procedimiento de utilizarse un término para referirse a algo ya enunciado.
Se puede identificar la anáfora en el siguiente ejemplo:
Una explicación que se presenta para esa sorpresa se basa en el siguiente hecho relacionado al país:
El autor trae al texto la voz de Dilma Rousseff, destacándola por un recurso gráfico, las comillas. En ese contexto, el uso de las comillas objetiva identificar el procedimiento de:

Na situação apresentada nos quadrinhos, as distâncias, em quilômetros, dAB, dBC e dCD formam, nesta ordem, uma progressão aritmética.
O vigésimo termo dessa progressão corresponde a:
Na imagem da etiqueta, informa-se o valor a ser pago por 0,256 kg de peito de peru.

O valor, em reais, de um quilograma desse produto é igual a:
De acordo com o esquema, os eixos dos recipientes estão contidos no segmento TQ, perpendicular ao plano horizontal β.
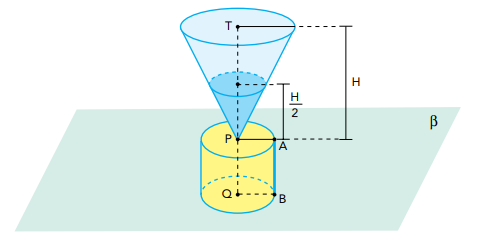
Admita que o funil esteja completamente cheio do óleo a ser escoado para o recipiente cilíndrico vazio. Durante o escoamento, quando o nível do óleo estiver exatamente na metade da altura do funil, H/2 , o nível do óleo no recipiente cilíndrico corresponderá ao ponto K na geratriz AB.
A posição de K, nessa geratriz, é melhor representada por:
Na tabela abaixo, estão indicadas três possibilidades de arrumar n cadernos em pacotes:
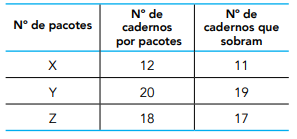
Se n é menor do que 1200, a soma dos algarismos do maior valor de n é:
Uma loja identifica seus produtos com um código que utiliza 16 barras, finas ou grossas. Nesse sistema de codificação, a barra fina representa o zero e a grossa o 1. A conversão do código em algarismos do número correspondente a cada produto deve ser feita de acordo com esta tabela:

Observe um exemplo de código e de seu número correspondente:


Esse código corresponde ao seguinte número:
Uma loja identifica seus produtos com um código que utiliza 16 barras, finas ou grossas. Nesse sistema de codificação, a barra fina representa o zero e a grossa o 1. A conversão do código em algarismos do número correspondente a cada produto deve ser feita de acordo com esta tabela:

Observe um exemplo de código e de seu número correspondente:

Observe no gráfico a função logaritmo decimal definida por y = log(x).
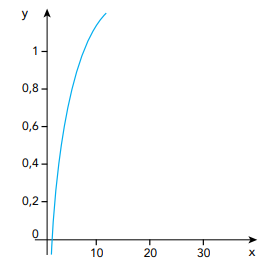
Admita que, no eixo x, 10 unidades correspondem a 1 cm e que, no eixo y, a ordenada log(1000) corresponde a 15 cm.
A escala x:y na qual os eixos foram construídos equivale a:



