Questões de Vestibular UNICENTRO 2016 para Vestibular - Química
Foram encontradas 15 questões
I. C(s) + O2(g) → CO(g) ∆H° = − 110,0kJ
II. C(s) + O2(g) → CO2(g) ∆H° = − 394,0kJ
III. CO(g) + O2(g) → CO2(g)
Os conversores catalíticos dos veículos automotores são dispositivos usados para reduzir as emissões nocivas de poluentes atmosféricos. Nas grandes cidades, a dispersão de gases tóxicos torna-se potencialmente grave para a população, principalmente idosa e infantil. Atualmente, o uso de sistemas de injeção eletrônica e de catalisadores, nos escapamentos diminuem o lançamento de poluentes para a atmosfera. Os catalisadores aceleram reações químicas que transformam poluentes, como o monóxido de carbono, CO(g), em dióxido de carbono, CO2(g), menos prejudiciais à saúde.
Considerando-se essas informações e com base nos
conhecimentos de química, é correto concluir:
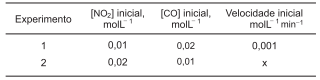
NO2(g) + CO(g) → CO2(g) + NO(g)
A Lei da velocidade de uma reação química é determinada, experimentalmente, porque, em geral, as reações ocorrem em duas ou mais etapas, e não diretamente como sugere a equação química. A reação química entre NO2(g) e CO(g) não é elementar, portanto ocorre em mais de uma etapa e tem Lei de velocidade representada pela expressão v = k[NO2] 2 , a 200° C.
Essas considerações e as informações da tabela permitem
corretamente concluir
Em um recipiente aberto, a água evapora até o fim, na temperatura e pressão ambiente. Entretanto, quando o recipiente é fechado, as moléculas de água são impedidas de escapar, ocorrendo, então, um equilíbrio de evaporação entre água líquida e vapor, a 25o°C e 1,0atm. Uma análise dessas informações permite corretamente concluir:
O balanceamento de equações químicas de oxirredução constitui ferramenta de grande utilidade na Química. O principal fundamento da técnica de balanceamento é o princípio de igualdade entre elétrons cedidos e recebidos, durante o processo de reação química. Considerando-se essas informações e a aplicação do princípio de balanceamento de equação química, com os menores coeficientes estequiométricos inteiros, é correto afirmar: