Questões de Vestibular UNIFESP 2007 para Vestibular - Conhecimentos Gerais
Foram encontradas 5 questões
Ano: 2007
Banca:
VUNESP
Órgão:
UNIFESP
Prova:
VUNESP - 2007 - UNIFESP - Vestibular - Conhecimentos Gerais |
Q218448
Química
A geração de lixo é inerente à nossa existência, mas a destinação do lixo deve ser motivo de preocupação de todos. Uma forma de diminuir a grande produção de lixo é aplicar os três R (Reduzir, Reutilizar e Reciclar). Dentro desta premissa, o Brasil lidera a reciclagem do alumínio, permitindo economia de 95% no consumo de energia e redução na extração da bauxita, já que para cada kg de alumínio são necessários 5 kg de bauxita. A porcentagem do óxido de alumínio 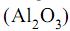 extraído da bauxita para produção de alumínio é aproximadamente igual a
extraído da bauxita para produção de alumínio é aproximadamente igual a
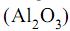 extraído da bauxita para produção de alumínio é aproximadamente igual a
extraído da bauxita para produção de alumínio é aproximadamente igual a
Ano: 2007
Banca:
VUNESP
Órgão:
UNIFESP
Prova:
VUNESP - 2007 - UNIFESP - Vestibular - Conhecimentos Gerais |
Q218449
Química
As lâmpadas fluorescentes estão na lista de resíduos nocivos à saúde e ao meio ambiente, já que essas lâmpadas contêm substâncias, como o mercúrio (massa molar 200 g/mol), que são tóxicas. Ao romper-se, uma lâmpada fluorescente emite vapores de mercúrio da ordem de 20 mg, que são absorvidos pelos seres vivos e, quando lançadas em aterros, contaminam o solo, podendo atingir os cursos d´água. A legislação brasileira estabelece como limite de tolerância para o ser humano 0,04 mg de mercúrio por metro cúbico de ar. Num determinado ambiente, ao romper-se uma dessas lâmpadas fluorescentes, o mercúrio se difundiu de forma homogênea no ar, resultando em 3,0 × 1017 átomos de mercúrio por metro cúbico de ar. Dada a constante de Avogadro 6,0 × 1023 mol –1, pode-se concluir que, para este ambiente, o volume de ar e o número de vezes que a concentração de mercúrio excede ao limite de tolerância são, respectivamente,
Ano: 2007
Banca:
VUNESP
Órgão:
UNIFESP
Prova:
VUNESP - 2007 - UNIFESP - Vestibular - Conhecimentos Gerais |
Q218450
Química
O índice de gasolina em não-conformidade com as especifi- cações da ANP (Agência Nacional de Petróleo, Gás Natural e Biocombustíveis) é um dado preocupante, já que alguns postos estavam vendendo gasolina com mais de 85% de álcool anidro. Todo posto de gasolina deve ter um kit para testar a qualidade da gasolina, quando solicitado pelo consumidor. Um dos testes mais simples, o “teste da proveta”, disposto na Resolução ANP n.º 9, de 7 de março de 2007, é feito com solução aquosa de cloreto de sódio (NaCl), na concentração de 10% p/v (100 g de sal para cada litro de água). O teste consiste em colocar 50 mL de gasolina numa proveta de 100 mL com tampa, completar o volume com 50 mL da solução de cloreto de sódio, misturar por meio de 10 inversões e, após 15 minutos de repouso, fazer a leitura da fase aquosa. O cálculo do teor de álcool é determinado pela expressão:
T = (A × 2) + 1, onde:
T: teor de álcool na gasolina, e
A: aumento em volume da camada aquosa (álcool e água).
O teste aplicado em uma amostra X de gasolina de um determinado posto indicou o teor de 53%. O volume, em mL, da fase aquosa obtida quando o teste foi realizado corretamente com a amostra X foi
T = (A × 2) + 1, onde:
T: teor de álcool na gasolina, e
A: aumento em volume da camada aquosa (álcool e água).
O teste aplicado em uma amostra X de gasolina de um determinado posto indicou o teor de 53%. O volume, em mL, da fase aquosa obtida quando o teste foi realizado corretamente com a amostra X foi
Ano: 2007
Banca:
VUNESP
Órgão:
UNIFESP
Prova:
VUNESP - 2007 - UNIFESP - Vestibular - Conhecimentos Gerais |
Q218454
Química
Amostras dos gases oxigênio e dióxido de enxofre foram coletadas nos frascos idênticos A e B, respectivamente. O gás trióxido de enxofre pode se formar se ocorrer uma reação entre os gases dos frascos A e B, quando estes são misturados em um frasco C.
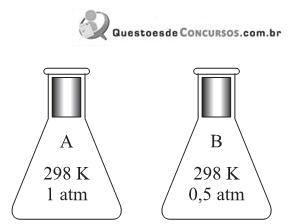
Sobre esses gases, são feitas as seguintes afirmações:
I. O frasco A apresenta o dobro de moléculas em relação ao frasco B.
II. O número de átomos do frasco B é o dobro do número de átomos do frasco A.
III. Ambos os frascos, A e B, apresentam a mesma massa.
IV. Considerando que a reação ocorreu por completo, o frasco C ainda contém gás oxigênio.
São corretas as afirmações

Sobre esses gases, são feitas as seguintes afirmações:
I. O frasco A apresenta o dobro de moléculas em relação ao frasco B.
II. O número de átomos do frasco B é o dobro do número de átomos do frasco A.
III. Ambos os frascos, A e B, apresentam a mesma massa.
IV. Considerando que a reação ocorreu por completo, o frasco C ainda contém gás oxigênio.
São corretas as afirmações
Ano: 2007
Banca:
VUNESP
Órgão:
UNIFESP
Prova:
VUNESP - 2007 - UNIFESP - Vestibular - Conhecimentos Gerais |
Q218455
Química
O gráfico apresenta a curva da decomposição térmica do oxalato de magnésio, 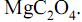 Nessa reação os produtos da decomposição são CO,
Nessa reação os produtos da decomposição são CO, 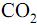 e MgO (massa molar 40 g/mol). Neste gráfico são apresentados os valores da massa da amostra em função da temperatura.
e MgO (massa molar 40 g/mol). Neste gráfico são apresentados os valores da massa da amostra em função da temperatura.
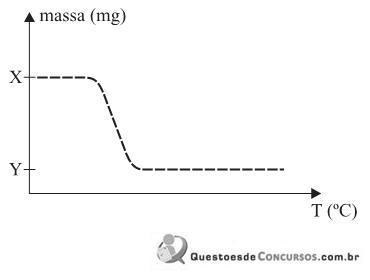
Se a diferença entre as massas X e Y no gráfico for 576 mg, o valor de Y e a porcentagem de perda da massa da reação de decomposição térmica do oxalato de magnésio são, respectivamente,
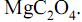 Nessa reação os produtos da decomposição são CO,
Nessa reação os produtos da decomposição são CO, 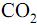 e MgO (massa molar 40 g/mol). Neste gráfico são apresentados os valores da massa da amostra em função da temperatura.
e MgO (massa molar 40 g/mol). Neste gráfico são apresentados os valores da massa da amostra em função da temperatura.
Se a diferença entre as massas X e Y no gráfico for 576 mg, o valor de Y e a porcentagem de perda da massa da reação de decomposição térmica do oxalato de magnésio são, respectivamente,