Questões de Vestibular UNIFESP 2007 para Vestibular - Conhecimentos Gerais
Foi encontrada 1 questão
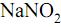 é um dos aditivos mais utilizados na conservação de alimentos. É um excelente agente antimicrobiano e está presente em quase todos os alimentos industrializados à base de carne, tais como presuntos, mortadelas, salames, entre outros. Alguns estudos indicam que a ingestão deste aditivo pode proporcionar a formação no estômago de ácido nitroso e este desencadear a formação de metabólitos carcinogênicos.
é um dos aditivos mais utilizados na conservação de alimentos. É um excelente agente antimicrobiano e está presente em quase todos os alimentos industrializados à base de carne, tais como presuntos, mortadelas, salames, entre outros. Alguns estudos indicam que a ingestão deste aditivo pode proporcionar a formação no estômago de ácido nitroso e este desencadear a formação de metabólitos carcinogênicos.Dada a constante de hidrólise:
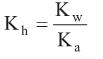
e considerando as constantes de equilíbrio
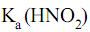 = 5 × 10–4 e
= 5 × 10–4 e 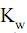 = 1 × 10–14, a 25 oC, o pH de uma solução aquosa de nitrito de sódio 5 × 10–2 mol/L nesta mesma temperatura tem valor aproximadamente igual a
= 1 × 10–14, a 25 oC, o pH de uma solução aquosa de nitrito de sódio 5 × 10–2 mol/L nesta mesma temperatura tem valor aproximadamente igual a