Questões de Vestibular Comentadas por alunos sobre química orgânica em química
Foram encontradas 850 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
II. Transporte e armazenamento. III. Sustentação mecânica. IV. Geração e transmissão de impulsos nervosos. V. Contração de células e produção de movimento. São funções exercidas pelas proteínas:
Os tocoferóis são conhecidos por sua ação antioxidante e estão presentes na maioria dos óleos vegetais.
Existem quatro tipos de tocoferóis, α, β, γ e δ, conforme mostrado a seguir:
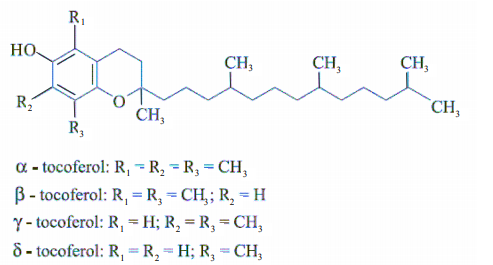
É INCORRETO afirmar que:




Pode-se concluir corretamente que, na combustão completa de 1 mol desse hidrocarboneto, as quantidades de matéria, e CO2 e de H2O produzidas são, em mol, respectivamente, iguais a