Questões de Vestibular
Foram encontradas 548 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Equação 1: 3C2H6(g) + 2HgO(s) + 5/2 O2(g) → 2(CH3)2Hg(g) + 2CO2(g) + 3H2O(g)
Equação 2: 3C2H5OH(g) + HgO(s) + 5O2(g) → (CH3)2Hg(g) + 4CO2(g) + 6H2O(g)
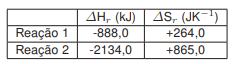
Com base no texto, nos conhecimentos sobre termodinâmica e cinética química, e supondo a queima total de HgO a 1 atm e a 300 K, assinale a alternativa correta.
I. A velocidade de uma reação é uma grandeza que indica como as quantidades de reagentes e produtos dessa reação variam em uma escala temporal. II. A velocidade das reações química depende da concentração dos reagentes. III. Quanto maior for a concentração de reagentes, menor será a velocidade das reações químicas. IV. Em uma reação química, a energia de ativação corresponde ao valor mínimo de energia que as moléculas de reagentes devem possuir para que seja eficaz uma colisão entre elas. V. O valor específico da energia de ativação em uma reação química é uma constante comum a todos os tipos de reações que podem ocorrer. VI. O aumento da temperatura, em uma reação química, contribui para o aumento da velocidade desta reação. VII. Uma substância caracterizada como catalisadora, aumenta a velocidade de uma reação química e, portanto, será, sem exceções, consumida durante a reação. VIII. Um catalisador aumenta a velocidade de uma reação química, pois promove aumento da energia de ativação da mesma. IX. Em uma reação química, a alteração na velocidade devido à ação de um catalisador é denominado catálise.
Na correção dessas afirmações feitas pelo aluno na prova, o professor descontou 2 pontos por cada afirmação incorreta. Sendo assim, pode-se considerar que foi descontado na prova do referido aluno:
DADOS QUE PODEM SER USADOS NESTA QUESTÃO

DADOS QUE PODEM SER USADOS NESTA QUESTÃO

4Fe(s) + 4NaCℓO3(s) → 2Fe2O3(s) + 4NaCℓ(s) + 3O2(g) + calor.
A proporção adequada entre as massas dos dois reagentes para que a reação ocorra sem sobra de nenhum deles é