Questões de Vestibular
Foram encontradas 584 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
SOLUÇÃO PARA A CRISE HÍDRICA PASSA PELO TRATAMENTO DA ÁGUA QUE VOLTA AO SISTEMA
Quando entregue, a água é utilizada para diferentes fins, desde limpeza, higiene pessoal, consumo ou processos industriais. Mesmo utilizada em todos esses processos, ela não desaparece. Estima-se que, do total de água entregue, são consumidos ou evaporados apenas 11,2 metros cúbicos por segundo (20% da água entregue). E o restante? Qual é a destinação desta água? O que fazemos com ela? O fato é que, se não se perde, não é consumida ou evaporada, esta água retorna ao sistema, seja como efluente, seja como esgoto. Esse volume representa quase 65% de toda água bruta que chega ao sistema de abastecimento.
Disponível em:
http://ineam.com.br/solucao-para-a-crise-hidrica-passa-pelo-tratamento-da-agua-que-volta-ao-sistema/.
Acesso em: 15 de agosto de 2015. (Adaptado)
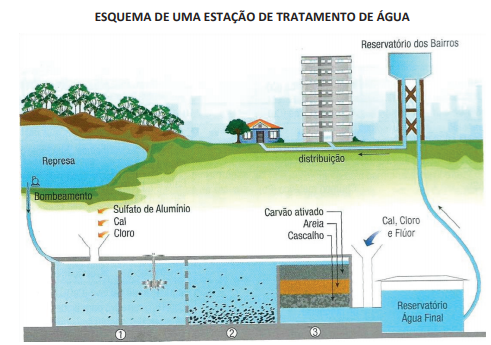
De acordo com o esquema apresentado de uma estação de
tratamento, depreende-se que os nomes dos processos de
separação mostrados nas etapas 2 e 3 e o produto obtido na
reação entre a cal virgem e a água são, respectivamente,
Considere a dissolução do cloreto de cálcio, utilizado para compressas quentes.
CaCl 2(s) + H2O(l) → Ca2+ (aq) + 2 Cl – (aq). ∆H = - 82,8 kJ / mol.
A dissolução de 1,0 mol de CaCl 2(s) libera 82,8 kJ de energia. Esse calor eleva a temperatura de 1,0 L de água de 20°C para 40°C. A dissolução de 0,5 mol de CaCl 2(s) em 1,0 L de água eleva a temperatura de 20°C para
A água oxigenada é utilizada como agente antisséptico devido à produção de gás oxigênio na sua decomposição, que ocorre conforme a equação
2H2O2(l) → 2H2O(l) + O2(g)
Essa equação indica que a espécie ganhadora de elétrons é
Dadas as equações químicas balanceadas:
Fe(s) ➜ Fe2+(aq) + 2e- (oxidação)
O2(g) + 2H2O(l) + 4e- ➜ 4OH- (redução)
A equação química balanceada que descreve a oxidação do ferro em meio aquoso neutro será:
Considere a equação química (não balanceada) para a combustão do etanol:
C2H6O(l) + O2(g) ➜ CO2(g) + H2O(l)
Dados: Entalpia de formação de C2H6O(l) = – 66 kcal/mol
Entalpia de formação de CO2(g) = – 94 kcal/mol
Entalpia de formação de H2O(l) = – 68 kcal/mol
A entalpia de combustão em kcal/mol será: