Questões de Vestibular
Foram encontradas 1.116 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
N2(g) + O2(g)

 2 NO(g)
2 NO(g) HCl(aq) + NaHCO3(aq) → NaCl(aq) + H2O(l) + CO2(g)↑
Considerando o volume de 1,0 L de fluido estomacal constituído somente por solução de HCl em pH 2, qual a massa aproximada de NaHCO3 necessária para aumentar o pH para 3?
Dados: Massas molares em g.mol−1 : H = 1; C = 12; O = 16; Na = 23; Cl = 35.
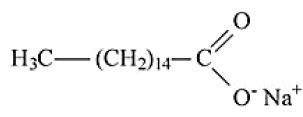
Em relação aos sabões, é CORRETO afirmar:
N2(g) + 3H2(g) ⇌ 2NH3(g) ∆H° = -92,6 KJ.mol-1
Um aluno, analisando a equação fornecida, fez as seguintes afirmações:
I - É possível maximizar a produção de amoníaco se a reação ocorrer a pressões elevadas. II - Dada a natureza exotérmica da reação direta, quanto menor a temperatura do vaso reacional, maior será a produção de amoníaco.
A alternativa CORRETA é:
