Questões de Vestibular
Foram encontradas 279 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!

Uma
das consequências do aumento do dióxido de carbono na atmosfera é a
acidificação dos oceanos. Naturalmente, tem-se o equilíbrio químico entre o
dióxido de carbono da atmosfera e o dissolvido nos oceanos. Com o aumento de
dióxido de carbono nas águas oceânicas esse equilíbrio é perturbado, e, logo,
organismos vivos constituídos, principalmente, de carbonato de cálcio, são
prejudicados.
Sobre o aumento da acidez nos oceanos e as suas
consequências, analise as proposições.
I. A
acidificação dos oceanos ocorre devido à reação química entre o gás carbônico
dissolvido e a água, resultando na formação do ácido carbônico cuja fórmula
química é HCO3.
II. Os
íons carbonatos provenientes do equilíbrio do carbonato de cálcio reagem com os
íons H+ gerados pelo ácido carbônico,
a fim de compensar o excesso de acidez gerado no oceano.
III. O
caráter mais ácido dos oceanos favorece a descalcificação dos exoesqueletos dos
corais, assim como dificulta a formação de novas estruturas de carbonato de
cálcio.
Assinale
a alternativa correta.
Em uma aula de laboratório de química, foi realizado um experimento que consistiu em adicionar em um béquer 300 g de água, em temperatura ambiente, e certa quantidade do sal sulfato de magnésio hexaidratado (MgSO4 . 6H2O) até formar uma solução saturada com corpo de fundo. Essa mistura foi aquecida até completa solubilização do sal, que ocorreu quando a temperatura atingiu 50 ºC. Na sequência, deixou-se a solução resfriar até 20 ºC e verificou-se novamente a presença do sal cristalizado no fundo do béquer.
Foram fornecidos aos alunos os dados de solubilidade desse sal nas duas temperaturas medidas.
Com as informações fornecidas, foram calculadas as massas do sal presente na solução a 50 ºC e do sal cristalizado
a 20 ºC. Esses resultados são corretamente apresentados,
nessa ordem, em:
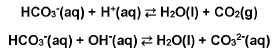
Ao adicionar carbonato de sódio na água de uma piscina, que está em condições consideradas adequadas para o banho, ocorrerá:
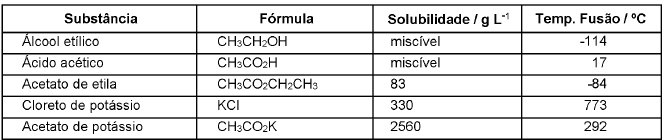
Qual das substâncias acima é a adequada para se preparar a solução de preenchimento desse tipo de extintor?
Os fertilizantes utilizados na reposição dos elementos químicos indispensáveis para o desenvolvimento dos vegetais são constituídos por sais inorgânicos, como o nitrato de potássio, KNO3(s), hidrogeno-fosfato de cálcio, CaHPO4(s), cloreto de amônio, NH4Cl(s), dentre outros. Os nutrientes são absorvidos pelas raízes das plantas sob a forma de íons, obtidos pela dissolução dos sais na água retida no solo, e dependem do pH do ambiente.
Com base nas informações associadas às estruturas e às propriedades dos sais inorgânicos, é correto afirmar