Questões de Vestibular
Foram encontradas 1.865 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
N2(g) + 3H2(g) ⇌ 2NH3(g) ∆H° = -92,6 KJ.mol-1
Um aluno, analisando a equação fornecida, fez as seguintes afirmações:
I - É possível maximizar a produção de amoníaco se a reação ocorrer a pressões elevadas. II - Dada a natureza exotérmica da reação direta, quanto menor a temperatura do vaso reacional, maior será a produção de amoníaco.
A alternativa CORRETA é:
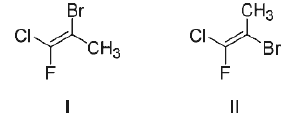
Em relação aos compostos apresentados, é CORRETO afirmar:
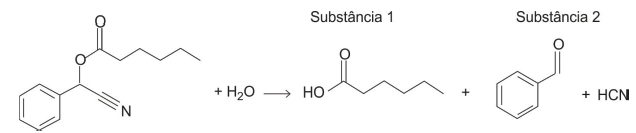
A cadeia carbônica da substância 1 é classificada como __________________ e __________________ . A oxidação da substância 2 resulta em um composto que pertence à função orgânica __________________ .
As lacunas são preenchidas, respectivamente, por
CaO (s) + 3C (s) → CaC2 (s) + CO (g)
Em um experimento em um reator aberto, verificou-se que a diferença entre a massa da mistura reacional e a massa do conteúdo no reator ao término da reação foi 1 400 g.
Dados: massa molar C = 12 g/mol massa molar O = 16 g/mol massa molar Ca = 40 g/mol
A massa de carbono que reagiu foi igual a
