Questões de Vestibular Comentadas por alunos sobre equilíbrio químico em química
Foram encontradas 270 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
O pH de uma solução que contém um precipitado de Cr(OH)3 (Kps = 6.0 x 10-11 a uma dada temperatura) deve ser ajustado de modo que todo o precipitado se dissolva, produzindo uma solução na qual a [Cr3+] seja 0.1 mol/L.
Nesse caso, o valor do pH é de, aproximadamente:
Dado: Kw = 1.0x 10-14
O hidróxido de alumínio (Al(OH)3), ao precipitar em solução aquosa, forma um sólido gelatinoso que pode ser usado como agente floculante no tratamento de água. Essa precipitação pode ocorrer pela adição de um hidróxido solúvel a uma solução aquosa ácida contendo um sal de alumínio solúvel, como o AlCl3. Entretanto, adicionando-se excesso de hidróxido ao meio, há a formação de íons Al(OH)4− , espécie solúvel em água, e o precipitado se solubiliza novamente. Dessa forma, dependendo do pH do meio, uma dentre as espécies Al(OH)4 −(aq), Al(OH)3(s) e Al 3+(aq) estará presente na solução em quantidade maior que as demais, como exemplificado no esquema.
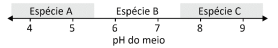
A alternativa que mostra corretamente qual das espécies estará
em quantidade maior que as duas outras em cada faixa de pH é:
Cálculos renais, conhecidos popularmente por “pedras nos rins”, consistem principalmente em oxalato de cálcio, CaC2O4, espécie cuja constante de solubilidade (Kps) é de aproximadamente 2 × 10−9 . Os íons oxalato, presentes em muitos vegetais, reagem com os íons cálcio para formar oxalato de cálcio, que pode gradualmente se acumular nos rins. Supondo que a concentração de íons cálcio no plasma sanguíneo seja de cerca de 5 × 10−3 mol/L, qual seria a concentração mínima, em mol/L, de íons oxalato para que CaC2O4 precipitasse?
Note e adote:
Desconsidere a presença de quaisquer
outros íons e considere que a
concentração no plasma é determinante
para a precipitação do oxalato.
(Disponível em:<http://www.usp.br/qambiental/chuva_acidafront.html#formacao>. Acesso em: 07 de nov. 2018. Adaptado).
Esse processo pode ser descrito por:
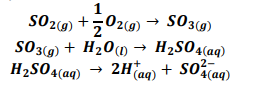
Uma amostra de chuva, contendo exclusivamente ácido sulfúrico (a = 100%), mostrou uma concentração de 5.10-5 mol /L.
O pH da referida chuva é de:
DADOS QUE PODEM SER USADOS NESTA PROVA
