Questões de Vestibular
Foram encontradas 450 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!

Observe a pilha eletroquímica representada no esquema a seguir.
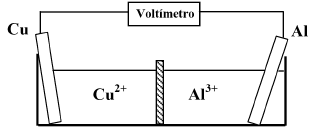
Dados:
Al3+/Al = - 1,66V
Cu2+/Cu= +0,34V
Sobre o seu funcionamento, assinale a opção incorreta.
A pilha de mercúrio é popularmente conhecida como pilha em forma de “botão” ou “moeda”, muito utilizada em calculadoras, controles remotos e relógios. Nessa pilha existe um amálgama de zinco (zinco dissolvido em mercúrio), óxido de mercúrio (II), e o eletrólito é o hidróxido de potássio. A partir das semirreações de redução do zinco e do mercúrio e seus respectivos potenciais padrão de redução, mostrados no quadro abaixo, assinale a alternativa que represente a pilha de mercúrio corretamente:

Os banhos eletrolíticos que fazem revestimento metálico têm uma sequência: uma peça para ser cromada necessariamente precisa ser primeiro cobreada, depois niquelada e, por fim, receber uma camada de crômio. [...] A deposição eletrolítica pode levar à produção de peças prateadas e douradas, além de outras onde ocorre estanhagem, cadmiagem e latonagem.
(LUFTI, M. Os ferrados e os cromados, produção social e apropriação privada do conhecimento químico. 2ºed. Ijuí: Ed. Unijuí, 2005. p. 110.)
Sobre o processo descrito acima, assinale a alternativa CORRETA:
H2CO3(aq) + Ca(OH)2(aq) → CaCO3(s) + 2 H2O(l) Equação 1
São apresentadas as entalpias-padrão de reação, em kJmol-1 , para três reações a 25oC:
I - CaO(s) + CO2(g) → CaCO3 (s) ΔH° = -183,3 kJmol-1 Equação 2 II - CaO (s) + H2O(l) → Ca(OH)2(aq) ΔH° = - 82,4 kJmol-1 Equação 3 III - CO2 (g) + H2O(l) → H2CO3(aq) ΔH° = - 20,5 kJmol-1 Equação 4
O valor da entalpia-padrão, em kJ, para a produção do carbonato na reação da equação 1 é: