Questões de Vestibular
Foram encontradas 1.155 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
 Oliver Sacks, Tio Tungstênio: Memórias de uma infância química.
Oliver Sacks, Tio Tungstênio: Memórias de uma infância química. De acordo com o autor,
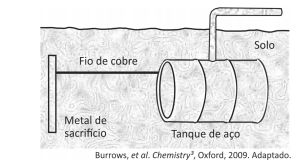
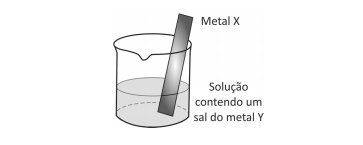
Um experimento para identificar quais metais podem ser utilizados como metal de sacrifício consiste na adição de um pedaço de metal a diferentes soluções contendo sais de outros metais, conforme ilustrado, e cujos resultados são mostrados na tabela. O símbolo ( + ) indica que foi observada uma reação química e o ( - ) indica que não se observou qualquer reação química.
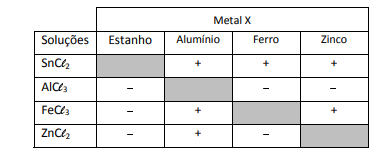 Da análise desses resultados, conclui-se que pode(m) ser
utilizado(s) como metal(is) de sacrifício para tanques de aço:
Da análise desses resultados, conclui-se que pode(m) ser
utilizado(s) como metal(is) de sacrifício para tanques de aço: Note e adote: o aço é uma liga metálica majoritariamente formada pelo elemento ferro.
6 CO2 (g) + 6 H2O (g) → C6H12O6 (aq) + 6 O2 (g) C6H12O6 (aq) → 2 C2H5OH (l) + 2 CO2 (g) ∆H = -70 kJ/mol C2H5OH (l)+ 3 O2 (g) → 2 CO2 (g) + 3 H2O (g) ∆H = -1.235 kJ/mol
Com base nessas informações, podemos afirmar que o valor de ∆H para a reação de fotossíntese é
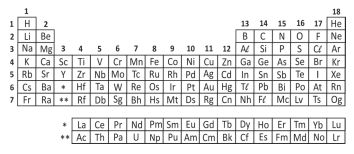
Analise a tabela periódica e as seguintes afirmações a respeito do elemento químico enxofre (S):
I. Tem massa atômica maior do que a do selênio (Se).
II. Pode formar com o hidrogênio um composto molecular de fórmula H2S.
III. A energia necessária para remover um elétron da camada mais externa do enxofre é maior do que para o sódio (Na).
IV. Pode formar com o sódio (Na) um composto iônico de fórmula Na3S.
São corretas apenas as afirmações