Questões de Vestibular
Foram encontradas 450 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
A base de uma escultura é formada por uma placa de latão, uma liga metálica de zinco (Zn) e cobre (Cu). Para minimizar os problemas relacionados à corrosão provocada pela chuva ácida, a placa foi recoberta com uma fina camada de prata (Ag). O recobrimento foi realizado a partir da eletrólise de uma solução aquosa de AgCl, fixando-se a placa de latão no anodo da célula eletrolítica. A voltagem foi ajustada de forma a se obter corrente constante de 10,0 A.

Átomos de Cu-63 e de Zn-65 têm a mesma quantidade de nêutrons.
A base de uma escultura é formada por uma placa de latão, uma liga metálica de zinco (Zn) e cobre (Cu). Para minimizar os problemas relacionados à corrosão provocada pela chuva ácida, a placa foi recoberta com uma fina camada de prata (Ag). O recobrimento foi realizado a partir da eletrólise de uma solução aquosa de AgCl, fixando-se a placa de latão no anodo da célula eletrolítica. A voltagem foi ajustada de forma a se obter corrente constante de 10,0 A.

Considerando as informações acima e assumindo que a constante de Faraday seja igual a 96.500 C/mol e que os únicos produtos formados nos eletrodos da célula eletrolítica sejam O2(g) e Ag(s), julgue o item seguinte.
Na eletrólise descrita, o tempo necessário para a deposição de
10,79 g de Ag é superior a 600 s.
Considere as seguintes afirmações a respeito de pilhas eletroquímicas, nas quais uma reação química produz um fluxo espontâneo de elétrons.
I - Os elétrons fluem, no circuito externo, do ânodo para o cátodo.
II - Os cátions fluem, numa ponte salina, do cátodo para o ânodo.
III- A reação de oxidação ocorre no cátodo.
Quais estão corretas?
Considere a reação de hidrogenação do ciclopenteno, em fase gasosa, formando ciclopentano, e a tabela de entalpias de ligação, mostradas abaixo.
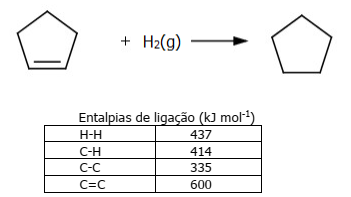
Qual será o valor da entalpia da reação de hidrogenação do ciclopenteno em kJ/mol?
Duas reações químicas envolvendo o gás metano, juntamente com o seu efeito térmico, são equacionadas abaixo.
C(graf) + 2 H2 (g) → CH4 (g) ΔHI
CH4 (g) + 2O2 (g) → CO2 (g) + 2H2O (l) ΔHII
Considere as seguintes afirmações a respeito das reações químicas.
I - ΔHI é um exemplo de entalpia de ligação.
II - ΔHII é um exemplo de entalpia de combustão.
III- ΔHII é negativo.
Quais estão corretas?