Questões de Vestibular Comentadas por alunos sobre representação das transformações químicas em química
Foram encontradas 434 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
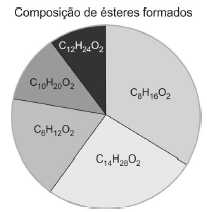
O ácido carboxílico presente em maior quantidade na amostra analisada é o:
Um certo polímero é produzido a partir de um monômero, que é um hidrocarboneto que contém somente uma instauração. A análise elementar por combustão completa de 0,5 mol de moléculas desse hidrocarboneto resultou em 1,5 mol de moléculas de CO2 .
A massa molar, em g.mol–1 , desse monômero é
Os palitos de fósforo são dispositivos simples empregados para fazer fogo. A chama se produz por meio de reações que ocorrem com as substâncias da “cabeça” do palito. Quando o palito é esfregado na superfície áspera da lateral da caixa, as substâncias reagem formando Sb2 O5 , KCl e SO2 . Essa reação é muito exotérmica e rápida e promove a reação de combustão e a propagação da chama pela madeira do palito.
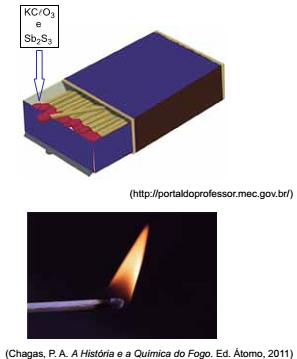
Equacionando-se e fazendo-se corretamente o balanceamento
da reação que ocorre pelo atrito da cabeça do palito de
fósforo com a lateral da caixa, a soma dos menores valores
inteiros dos coeficientes estequiométricos é
A bioluminescência é o fenômeno de emissão de luz visível por certos organismos vivos, resultante de uma reação química entre uma substância sintetizada pelo próprio organismo(luciferina) e oxigênio molecular, na presença de uma enzima (luciferase). Como resultado dessa reaçãobioquímica é gerado um produto em um estado eletronicamenteexcitado (oxiluciferina*). Este produto, por suavez, desativa-se por meio da emissão de luz visível, formandoo produto no estado normal ou fundamental (oxiluciferina).Ao final, a concentração de luciferase permanece constante.

O esquema ilustra o mecanismo geral da reação de bio-luminescência de vagalumes, no qual são formados dois produtos diferentes em estados eletronicamente excitados,responsáveis pela emissão de luz na cor verde ou na cor vermelha.

A luz branca é composta por ondas eletromagnéticas de todas as frequências do espectro visível. O espectro de radiação emitido por um elemento, quando submetido a um arco elétrico ou a altas temperaturas, é descontínuo e apresenta uma de suas linhas com maior intensidade, o que fornece “uma impressão digital” desse elemento. Quando essas linhas estão situadas na região da radiação visível, é possível identificar diferentes elementos químicos por meio dos chamados testes de chama. A tabela apresenta as cores características emitidas por alguns elementos no teste de chama:
Elemento Cor
sódio laranja
potássio violeta
cálcio vermelho-tijolo
cobre azul-esverdeada