Questões de Vestibular
Foram encontradas 1.865 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
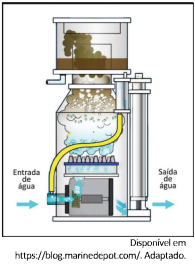
Em aquários de água marinha, é comum o uso do equipamento chamado "Skimmer", aparato em que a água recebe uma torrente de bolhas de ar, como representado na figura, levando a matéria orgânica até a superfície, onde pode ser removida. Essa matéria orgânica eliminada é composta por moléculas orgânicas com parte apolar e parte polar, enquanto as bolhas formadas têm caráter apolar. Esse aparelho, no entanto, tem rendimento muito menor em aquários de água doce (retira menos quantidade de material orgânico por período de uso).
Considerando que todas as outras condições são mantidas, o menor rendimento desse aparato em água doce do que em água salgada pode ser explicado porque
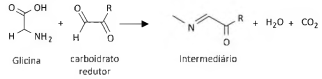
A reação de Maillard, que ocorre entre aminoácidos e carboidratos redutores, é a responsável por formar espécies que geram compostos coloridos que conferem o sabor característico de diversos alimentos assados. Um exemplo é a reação entre a glicina e um carboidrato redutor mostrada na equação em que R representa uma cadeia genérica:
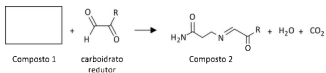
Um aminoácido específico (Composto 1), ao reagir com o carboidrato redutor, pode gerar o Composto 2, levando à formação de acrilamida, uma espécie potencialmente carcinogênica, conforme mostrado na equação:
A estrutura do aminoácido marcado como Composto 1 e que é
capaz de gerar esse intermediário de espécies carcinogênicas é:
Para estudar equilíbrio químico de íons Co2+ em solução, uma turma de estudantes realizou uma série de experimentos explorando a seguinte reação:
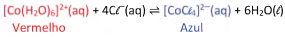
Nesse equilíbrio, o composto de cobalto com água, [Co(H2O)6]2+(aq), apresenta coloração vermelha, enquanto o composto com cloretos, [CoCl4]2-(aq), possui coloração azul.
Para verificar o efeito de ânions de diferentes sais nessa mudança de cor, 7 ensaios diferentes foram realizados. Aos tubos contendo apenas alguns mL de uma solução de nitrato de cobalto II, de coloração vermelha, foram adicionadas pequenas quantidades de diferentes sais em cada tubo, como apresentado na tabela, com exceção do ensaio 1, no qual nenhum sal foi adicionado.
Após agitação, os tubos foram deixados em repouso por um tempo, e a cor final foi observada.
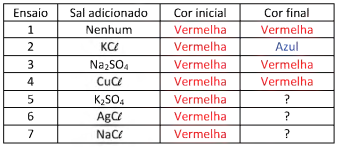
A alternativa que representa a cor final observada nos ensaios 5, 6 e 7, respectivamente, é:
Note e adote:
Solubilidade dos sais em g/100 mL de água a 20 °C
AgCℓ 1,9 x 10-4 NaCℓ 35,9
CuCℓ 9,9 x 10-3 Na2SO4 13,9
KCℓ 34,2 K2SO4 11,1
Observe a representação a seguir, em que os círculos brancos representam uma espécie química (molécula ou íon molecular) e os círculos coloridos, outra.
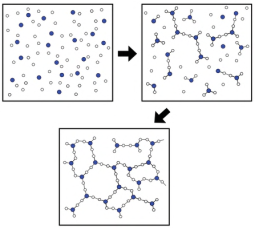
Essa representação pode ser corretamente associada à